اطلاعات اولیه
کروماتوگرافی تبادل یونی در ستونها ، بطور انحصاری ، کاربرد رزینهای تبادل یونی محدود میشود زیرا این مواد به طور عمده خواص مطلوبی ، مانند پایداری مکانیکی و شیمیایی و یکنواختی اندازه دانهها ( ذرات ) دارند، پودر سلولز که آن گردههای تبادل یونی به طریق شیمیایی قرار داده شده باشند نیز برای جداسازی مواد در ستونها به کار میرود. ورقههایی از سلولز عمل شده فوق و ورقههای سلولز پر شده با رزینهای تبادل یونی را در روش کروموتوگرافی کاغذی برای جداسازیهایی که شامل تبادل یونی هستند، میتوان مورد استفاده قرار داد.
توصیف
در کروماتوگرافی تبادل یونی جداسازی مواد از نوع کروماتوگرافی که در آنها رزین به جای جاذب در کروماتوگرافی جذبی قرار میگیرد، است. مقادیر زیادی از رزینهای تبادل یونی برای جدا کردن کامل یونها از محلول در آزمایشگاه و نیز در مقیاس صنعتی به کار میروند. یعنی از جداسازیهای فوق العاده جالب عبارتند از جداسازی مواد لانتایندها، آکتینیدها و اسیدهای آمینه.
رزینهای متداول تبادل یونی
رزینهای متداول تبادل یونی که به طور مصنوعی ساخته میشوند، بر پایه قالب غیر محلولی از یک بسپار بزرگ ، معمولا پلی استیرن ، استوار هستند. ولی بعضی از آنها متکی بر اسید متا اکریلیک هستند. نوع اول با بسپار کردن استیرن در حضور مقدار کمی از دی وینیل بنزن ساخته میشود. دی وینیل بنرن میزان اتصالات عرضی را که عامل مهمی در کروماتوگرافی است کنترل میکند. اتصالات عرضی ، بسپار را به حالت نامحلول در میآورد. اگر میزان اتصالات عرضی خیلی کم باشد رزین مستعد جذب مایع اضافی میشود و در نتیجه آماس زیادی میکند، در حالی که اتصالات عرضی زیاده از حد ، ظرفیت تبادل رزین را ، احتمالا به علت ممانعت فضایی کم میکند.
گردههای قطبی که باعث خواص تبادل یون در رزین می شوند به جز در مورد اسید پلی متا اکریلیک، بعد از عمل بسپار شدن به رزین اضافه میشوند. با بسپار شدن در یک امولسیون آبی میتوان دانههایی با اندازههای معین تهیه کرد و در این صورت است که رزینها برای عمل یون زدایی و اهداف کروماتوگرافی به کار میروند. بعضی از رزینها را به شکل ورقه میسازند که در این صورت غشاهای تبادل یونی به دست میآیند. این غشاها به این صورت کاربردی در کروماتوگرافی ندارند ولی میتوان از آنها برای نمکزدایی محلولها ، که ممکن است یک عمل مقدماتی ضروری برای یک جداسازی مواد کروماتوگرافی مورد نظر باشد، استفاده کرد.
- مواد مبادله کننده یون : تبادل گرهای کاتیونی و آنیونی دو نوع عمده مواد مبادله کننده یون هستند که آنها را به نوبه خود میتوان بر حسب قدرتشان به اسید و باز تقسیمبندی کرد.
- تبادلگر کاتیونی : گروههای قطبی در تبادلگرهای کاتیونی، که یا
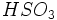 و یا
و یا  میباشند، خاصیت اسیدی دارند این گروهها به مولکولهای بسپار به طور قطعی متصل هستند و در معرض محلول حاوی یونهایی که باید حذف یا جدا شوند، قرار میگیرند.
میباشند، خاصیت اسیدی دارند این گروهها به مولکولهای بسپار به طور قطعی متصل هستند و در معرض محلول حاوی یونهایی که باید حذف یا جدا شوند، قرار میگیرند. - گروههای قطبی در تبادل گرهای آنیونی گروههای آمونیوم نوع سوم یا چهارم هستند و مثل هم عمل میکنند. تبادلگر آنیونی بیشتر به شکل کلرید هستند تا به شکل هیدروکسید زیرا کلریدها پایدارتر هستند.
خواص رزینها
- باید دارای گروههای مبادله کننده تک عاملی باشد. برای رزینهای جدید هیچ مشکلی در این مورد وجود ندارد ولی محصولات اولیه که از فنل ساخته میشدند چند عاملی بودند و خواص تبادل آنها بستگی به PH محلولی که در آن قرار میگرفتند، داشت. از این نقطه نظر این رزینها برای کروماتوگرافی مناسب نبودند.
- باید درجه اتصالات عرضی کنترل شده داشته باشد. 4 - 8 % بهترین درجه برای کروماتوگرافی است.
- گستره اندازه ذرات باید تا آنجایی که ممکن است کوچک باشد.
- اندازه ذرات باید، تا آنجایی که عملی است کوچک باشد.
مزیت اساسی کروماتوگرافی تبادل یونی
در کروماتوگرافی ، محلولهای بکار رفته اکثرا رقیق هستند و در نتیجه روش شستشو بیشتر به کار میرود و اغلب جداسازیهای بسیار رضایت بخشی به دست میآید. در مورد رزینها تجزیه جانشینی و تجزیه مرحلهای و شستشوی تدریجی همگی به کار میروند. ولی از تجزیه جبههای استفاده نمیشود. روش دیگر شستشو ، تحت عنوان گزینش پذیری ، نیز کارآیی مفیدی دارد. این روش به تغییر فعالیت یونهایی بستگی دارد که باید بوسیله عامل شویندهای که با یونها تشکیل کمپلکس میدهد جدا شوند.
تشکیل کمپکس بدون شک عامل مهمی در سایر روشهای کروماتوگرافی ، مخصوصا در جداسازیهای معدنی روی کاغذ است، ولی در هیچ یک از سایر روشها این موضوع به همان وسعت که در کروماتوگرافی تبادل یونی استفاده شده، مطالعه نشده است. یکی از قدیمیترین و جالبترین موفقیتها در کروماتوگرافی تبادل یونی جداسازی مواد لانتایندها در یک رزین اسید قوی و با استفاده از یک محلول سیترات تامپونی برای شستشو است.
کروماتوگرافی نمک زنی
در روش کروماتوگرافی نمکزنی ، از رزینهای تبادل یونی برای جداسازی مواد غیر الکترولیتها ، با شستن آنها از ستون به وسیله محلولهای آبی یک نمک ، استفاده میشود. اجسام جدا شده بوسیله این روش ، اترها ، آلدئیدها ، کتونها و آمینها هستند.
تبادلگرهای یون معدنی
بعضی از نمکهای معدنی برای پر کردن کاغذ و آماده سازی آن به منظور استفاده در جداسازیها که بر اثر تبادل یون صورت میگیرند، بکار میروند. یکی از دلایل توجه به مواد معدنی این است که تبادلگرهای یونی رزینی بر اثر تابش مستعد خراب شدن هستند. بنابراین در حقیقت برای استفاده با محلولهای خیلی فعال مناسب نیستند. اگر چه برای جداسازی مواد ، به عنوان مثال ، مخلوطهای اکتیندها یا موفقیت به کاربرده شدهاند. مواد معدنی دارای مزایای دیگری مانند گزینش پذیری خیلی زیاد برای بعضی از یونها مانند روبیدیم و سزیم و توانایی در برابر محلولهای با دمای بالا هستند.
به علاوه تبادل گرهای یونی معدنی وقتی که در آب قرار میگیرند به مقدار قابل توجهی آماس نمیکنند و حجم آنها با تغییر قدرت یونی محلول در تماس با آنها تغییر نمیکند. از طرف دیگر ، بعضی از مواد معدنی معایبی مانند انحلال پذیری یا والختی در بعضی از PHها که در آن معمولا رزینها پایدارند، دارند یا ممکن است در محلولهایی که رزینها غیر محلول هستند، حل شوند. همچنین تبادلگرهای یونی معدنی ممکن است به شکل بلورهای ریز باشند که به علت ممانعت از عبور فاز متحرک ، برای پر کردن در ستونها مناسب نیستند. اگر چه راههایی برای فائق آمدن به این مشکل وجود دارد.
برچسبها: کروماتوگرافی تبادل یونی, کروماتوگرافی, شیمی تجزیه
شراط تشکسل پیوند
شرط تشکیل پیوند کوولانسی
لازمه تشکیل پیوند کوولانسی بین دو اتم ، این است که هر یک از دو اتم در آخرین تراز انرژی خود لااقل یک اوربیتال نیمه پر داشته باشند.
شرط تشکیل پیوند داتیو
در تشکیل پیوند داتیو باید اتمی که الکترون به اشتراک میگذارد، در آخرین لایه ، حداقل یک جفت الکترون غیر پیوندی داشته باشد و اتم دیگر نیز حداقل دارای یک اوربیتال خالی در آخرین لایه باشد.
پیوند یافتن  با مولکول آمونیاک و تشکیل یون آمونیوم
با مولکول آمونیاک و تشکیل یون آمونیوم
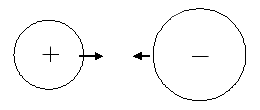
وقتی مولکول آمونیاک در محیطی با یون  مجاور شود، آن را به سوی قطب منفی خود که نیتروژن است، جذب مینماید و وقتی
مجاور شود، آن را به سوی قطب منفی خود که نیتروژن است، جذب مینماید و وقتی  که اوربیتال 1s آن خالی است، به قدر کافی به نیتروژن نزدیک شد، نیتروژن آمونیاک ، جفت الکترون غیر پیوندی خود را با یون
که اوربیتال 1s آن خالی است، به قدر کافی به نیتروژن نزدیک شد، نیتروژن آمونیاک ، جفت الکترون غیر پیوندی خود را با یون  به اشتراک میگذارد.
به اشتراک میگذارد.
باید توجه داشت که وقتی نیتروژن آمونیاک که دارای هیبرید 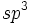 است، جفت الکترون غیر پیوندی خود را در اختیار یون
است، جفت الکترون غیر پیوندی خود را در اختیار یون  گذاشت، هنوز هم حالت هیبریدی آن
گذاشت، هنوز هم حالت هیبریدی آن 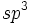 است، ولی دیگر چهار وجهی یون
است، ولی دیگر چهار وجهی یون  نامتقاون نیست، زیرا جفت الکترون غیر پیوندی نیتروژن که عامل نامتقارن کننده چهار وجهی آن بود، بکار گرفته شد و یون آمونیوم (
نامتقاون نیست، زیرا جفت الکترون غیر پیوندی نیتروژن که عامل نامتقارن کننده چهار وجهی آن بود، بکار گرفته شد و یون آمونیوم ( ) به صورت یک چهار وجهی متقارن با زوایای پیوندی '28،˚109 در میآید و شبیه
) به صورت یک چهار وجهی متقارن با زوایای پیوندی '28،˚109 در میآید و شبیه  ،
، 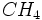 و ... میباشد.
و ... میباشد.
پیوند یافتن  با
با 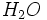 و تشکیل یون هیدرونیوم
و تشکیل یون هیدرونیوم
اکسیژن آب دارای دو جفت الکترون غیر پیوندی است و وقتی با یون  مجاور شود، آن را به سوی خود میکشد و با آن پیوند داتیو تشکیل میدهد و یون هیدرونیوم (
مجاور شود، آن را به سوی خود میکشد و با آن پیوند داتیو تشکیل میدهد و یون هیدرونیوم (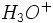 ) را بوجود میآورد. باید توجه داشت که اتم اکسیژن در یون هیدرونیوم هم دارای هیبرید
) را بوجود میآورد. باید توجه داشت که اتم اکسیژن در یون هیدرونیوم هم دارای هیبرید 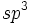 است، ولی چون یک جفت از الکترونهای غیر پیوندی آن بکار گرفته شده، نیروی دافعه وارد بر پیوندها نسبت به آن کمتر میشود، یعنی چهار وجهی آب نسبت به چهار وجهی یون هیدرونیوم نامتقارنتر است.
است، ولی چون یک جفت از الکترونهای غیر پیوندی آن بکار گرفته شده، نیروی دافعه وارد بر پیوندها نسبت به آن کمتر میشود، یعنی چهار وجهی آب نسبت به چهار وجهی یون هیدرونیوم نامتقارنتر است.
با اینکه هنوز یک جفت الکترون غیر پیوندی بر روی اکسیژن باقیمانده است، ولی نمیتواند با یون  دیگر ، یک پیوند داتیو دیگر تشکیل دهد و یون
دیگر ، یک پیوند داتیو دیگر تشکیل دهد و یون  را بوجود آورد. زیرا وقتی مولکول آب را با یون
را بوجود آورد. زیرا وقتی مولکول آب را با یون  پیوند داتیو تشکیل داد و به یون
پیوند داتیو تشکیل داد و به یون 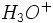 تبدیل شد، یون
تبدیل شد، یون  دیگر نمیتواند به این یون مثبت نزدیک شود، زیرا مجموعه
دیگر نمیتواند به این یون مثبت نزدیک شود، زیرا مجموعه 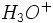 به علت داشتن بار مثبت ، آنها را از خود دور مینماید و شرط اول برقراری پیوند بین دو ذره که تماس آنها با هم است، برقرار نمیشود.
به علت داشتن بار مثبت ، آنها را از خود دور مینماید و شرط اول برقراری پیوند بین دو ذره که تماس آنها با هم است، برقرار نمیشود.
پیوند یافتن مولکول 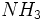 با مولکول
با مولکول 
وقتی مولکول 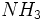 با
با  مجاور شود، اتم نیتروژن آمونیاک ، جفت الکترون غیر پیوندی خود را در اوبیتال خالی بور در
مجاور شود، اتم نیتروژن آمونیاک ، جفت الکترون غیر پیوندی خود را در اوبیتال خالی بور در  قرار میدهد و با آن پیوند داتیو برقرار میسازد.
قرار میدهد و با آن پیوند داتیو برقرار میسازد.
الکتروفیل و نوکلئوفیل
در شیمی به ذراتی مانند یون  که برای رسیدن به آرایش الکترونی گاز بی اثر به دو یا چند الکترون نیاز دارند و یا مولکولهایی مثل
که برای رسیدن به آرایش الکترونی گاز بی اثر به دو یا چند الکترون نیاز دارند و یا مولکولهایی مثل  که در آنها اتم مرکزی در آخرین لایه ، اوربیتال خالی دارد و برای رسیدن به آرایش گاز بی اثر به الکترون محتاج است و در واکنشها به نقاطی متمایل میشوند که دارای الکترون باشند، ذرات الکترون دوست یا الکتروفیل گفته میشود.
که در آنها اتم مرکزی در آخرین لایه ، اوربیتال خالی دارد و برای رسیدن به آرایش گاز بی اثر به الکترون محتاج است و در واکنشها به نقاطی متمایل میشوند که دارای الکترون باشند، ذرات الکترون دوست یا الکتروفیل گفته میشود.
ذراتی مثل 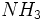 که در آنها اتم مرکزی دارای جفت الکتورن غیر پیوندی بوده و در صورت لزوم میتوانند جفت الکتورن خود را در اختیار اتم دیگر بگذارند و پیوند داتیو برقرار نمایند و در واکنشها به سوی نقاطی که دارای بار مثبت هستند، متمایل شوند، ذرات هسته دوست یا مثبت دوست یا نوکلئوفیل نامیده میشوند.
که در آنها اتم مرکزی دارای جفت الکتورن غیر پیوندی بوده و در صورت لزوم میتوانند جفت الکتورن خود را در اختیار اتم دیگر بگذارند و پیوند داتیو برقرار نمایند و در واکنشها به سوی نقاطی که دارای بار مثبت هستند، متمایل شوند، ذرات هسته دوست یا مثبت دوست یا نوکلئوفیل نامیده میشوند.
به این ترتیب تمام یونهای مثبت و مولکولهایی که اتم مرکزی آنها هنوز از نظر آرایش الکترونی شبیه گاز بی اثر نشده است، الکتروفیل هستند و تمام یونهای منفی و مولکولهایی که اتم مرکزی آنها دارای حداقل یک جفت الکترون غیر پیوندی است، نوکلئوفیل میباشند. الکتروفیلها مثل  ،
، 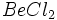 ،
، 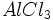 ،
،  ،
، 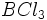 و ... ، نوکلئوفیلها مثل
و ... ، نوکلئوفیلها مثل 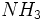 ،
، 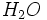 ، آمینها و الکلها و ... .
، آمینها و الکلها و ... .
عناصر گروههای مختلف و تشکیل پیوند داتیو
- عناصر گروه اصلی اول در تشکیل پیوند داتیو شرکت نمیکنند.
- عناصر گروه اصلی دوم پس از تشکیل مولکول در آخرین لایه ، 4 الکترون دارند. در صورتی که خصلت غیر فلزی داشته باشند، مثل Be در
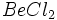 ، میتوانند با دو اوربیتال خالی باقیمانده خود به عنوان گیرنده الکترون در تشکیل دو پیوند داتیو با سایر ذرات شرکت نمایند. مثل مولکولهای
، میتوانند با دو اوربیتال خالی باقیمانده خود به عنوان گیرنده الکترون در تشکیل دو پیوند داتیو با سایر ذرات شرکت نمایند. مثل مولکولهای 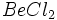 که وقتی در کنار هم قرار میگیرند، هر اتم Be با دو اتم کلر از دو مولکول مجاور خود ، 4 الکترون به صورت دو تا پیوند داتیو میگیرد و به همین دلیل همه مولکولهای
که وقتی در کنار هم قرار میگیرند، هر اتم Be با دو اتم کلر از دو مولکول مجاور خود ، 4 الکترون به صورت دو تا پیوند داتیو میگیرد و به همین دلیل همه مولکولهای 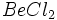 در حالت جامد به هم متصل هستند و
در حالت جامد به هم متصل هستند و 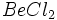 به جای اینکه از نوع جامد مولکولی باشد، از نوع جامد کووالانسی است.
به جای اینکه از نوع جامد مولکولی باشد، از نوع جامد کووالانسی است. - عناصر گروه اصلی سوم پس از تشکیل مولکول ، میتوانند با یک اوربیتال خالی آخرین لایه اتم خود ، به عنوان گیرنده دو الکترون در یک پیوند داتیو با سایر یونهای منفی یا مولکولها شرکت نمایند. مثل B در
 که با مولکول آمونیاک یک پیوند داتیو تشکیل داده است.
که با مولکول آمونیاک یک پیوند داتیو تشکیل داده است. - عناصر گروه اصلی چهارم نه به عنوان گیرنده الکترون و نه به عنوان دهنده الکترون در داتیو شرکت نمینمایند.
- عناصر گروه اصلی پنجم بعد از تشکیل مولکول و رسیدن به آرایش گاز بی اثر ، یک جفت الکترون غیر پیوندی دارند و میتوانند آن را به عنوان دهنده الکتون در یک پیوند داتیو شرکت دهند. مثل نیتروژن در آمونیاک.
- عناصر گروه اصلی ششم بعد از تشکیل مولکول و رسیدن به آرایش الکترونی گاز بی اثر ، دارای دو جفت الکترون غیر پیوندی هستند و حداکثر دو پیوند داتیو با سایر اتمها برقرار میسازند. مثل گوگرد در اسید سولفوریک.
- عناصر گروه اصلی هفتم یا هالوژنها حداکثر 3 پیوند داتیو میتوانند با سایر اتمها برقرار سازند. مثل کلر در اسید پرکلریک (
 ) که فرمول ساختمانی آن به صورت است.
) که فرمول ساختمانی آن به صورت است.
برچسبها: پیوند داتیو, پیوند کووالانسی, هیبریداسیون
| اتمهای گازهای بیاثر میل ندارند با عنصرهای دیگر پیوند تشکیل دهند یا با اتمهای دیگری از نوع خود به یکدیگر بپیوندند، ولی عنصرهای دیگر به جز گازهای بیاثر نمیتوانند به تنهایی و بدون پیوستن به اتمهای عنصرهای دیگر یا اتمهای دیگری از نوع خود به بقای خود ادامه دهند و حتما باید با اتم یا اتمهای دیگر پیوند تشکیل دهند. به هم پیوستن دو اتم را معمولا تشکیل پیوند میگویند. |
دید کلی
بررسی مواد ساده و مرکب در طبیعت نشان میدهد که اکثریت قریب به اتفاق اتمها در طبیعت به حالت آزاد وجود ندارند. مواد سادهای که در طبیعت به حالت آزاد وجود دارند، بندرت بصورت مولکول تک اتمیهستند. بیشتر مواد ساده بصورت مولکولهای دو یا چند اتمی در طبیعت پیدا میشوند. برای مثال گاز هیدروژنی که از اثر اسیدها بر فلزها یا از تجزیه الکتریکی آب یا از هر راه دیگری بدست میآید، بصورت مولکول دو اتمی 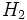 است.
است.
اکسیژن نیز در اغلب موارد بصورت مولکول دو اتمی 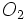 و گاهی نیز بصورت مولکول سه اتمی اوزون
و گاهی نیز بصورت مولکول سه اتمی اوزون 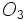 یافت میشود. فسفر سفید بصورت مولکول چهار اتمی
یافت میشود. فسفر سفید بصورت مولکول چهار اتمی 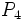 و گوگرد بصورت مولکول هشت اتمی
و گوگرد بصورت مولکول هشت اتمی  است. تنها گازهای بیاثر در طبیعت بصورت تک اتمی یافت میشوند.
است. تنها گازهای بیاثر در طبیعت بصورت تک اتمی یافت میشوند.
عکس پیدا نشد
پیوند شیمیایی در هیدروژن
وقتی دو اتم هیدروژن به یکدیگر نزدیک میشوند، اوربیتالهای اتمی آنها به یک اوربیتال مولکولی تبدیل میشود. در اوربیتال مولکولی ابر الکترونی تحت تاثیر جاذبه دو هسته قرار دارد. در حالی که در اوربیتال اتمی ابر الکترونی تحت تاثیر جاذبه یک هسته است.
چون نیروی جاذبه هستهها در فضای بین دو هسته از جاهای دیگر بیشتر است، در نتیجه تراکم ابر الکترونی در فاصله دو هسته از جاهای دیگر بیشتر خواهد بود.
انرژی پیوند
انرژی پیوند ، عبارت است از مقدار انرژی آزاد شده به هنگام تشکیل پیوند بین یک مول اتمهای گازی شکل یک عنصر با یک مول اتمهای گازی شکل همان عنصر یا عنصر دیگر.
انواع پیوند شیمیایی
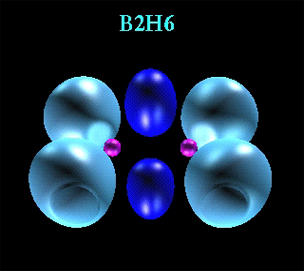
پیوند کووالانسی
در مولکول هیدروژن ، اتمها ، الکترون به اشتراک میگذارند و با استفاده از مدل بور ، الکترونهای مشترک بر روی مدار خارجی هر دو اتم گردش میکنند. به بیان دیگر ، ابر الکترونی تحت تاثیر جاذبه دو هسته قرار دارد و تراکم ابر الکترونی در فاصله دو هسته از جاهای دیگر بیشتر است. چنین پیوندی پیوند کووالانسی نامیده میشود.
پیوند کووالانسی بین دو اتم هیدروژن از همپوشانی اوربیتال s بوجود میآید و مولکول حاصل بیضوی است که هستههای دو اتم در دو کانون آن قرار دارند و تراکم ابر الکترونی در بین دو هسته زیاد و در اطراف هستهها کمتر است. در نتیجه تشکیل پیوند ، اوربیتالهای اتمی به اوربیتال مولکولی تبدیل میشوند. اوربیتالهای مولکولی حاصل از تشکیل پیوند میان دو اتم هیدروژن بیضوی است که تراکم ابر الکترونی بر روی خط واصل بین هستههای آن از جاهای دیگر بیشتر است. این شکل اوربیتال مولکولی اوربیتال مولکولی سیگما یا پیوند سیگما نامیده میشود.
در نوع دیگر از اوربیتالهای مولکولی ، نه تنها سطح انرژی پائین نمیآید و انرژی آزاد نمیشود، بلکه سطح انرژی از اتمهای اولیه نیز بالاتر است، این اوربیتال را نمیتوان اوربیتال پیوندی نامید، بلکه یک اوربیتالی ضد پیوندی است و بصورت 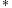 نشان داده میشود.
نشان داده میشود.
هرچه در یک مولکول ، تعداد اوربیتالهای پیوندی اشغال شده بیشتر باشد، مولکول پایدارتر است، ولی هر گاه تعداد اوربیتالهای پیوندی و ضد پیوندی برابر باشد، دو اتم از یکدیگر جدا میمانند و بین آنها پیوندی تشکیل نمیشود. تعداد پیوند میان دو اتم برابر نصف تعداد الکترونهای موجود در اوربیتالهای پیوندی منهای نصف تعداد الکترونهای موجود در اوربیتالهای ضد پیوندی است.
- پیوند اکسیژن با هیدروژن :
اکسیژن ، دو اوربیتال تک الکترونی دارد. هر گاه یک اتم اکسیژن و یک اتم هیدروژن به یکدیگر نزدیک شوند، امکان جاذبه بر دافعه وجود دارد و در این صورت پیوند تشکیل میشود. در این مجموعه ، هیدروژن به آرایش گاز بیاثر هلیم رسیده است، ولی اکسیژن در خارجیترین سطح انرژی خود دارای هفت الکترون شده و هنوز به آرایش گاز بیاثر نرسیده است.
آرایش الکترونی اکسیژن پس از تشکیل یک پیوند با یک هیدروژن مشابه آرایش الکترونی فلوئور شده است. بنابراین این مجموعه میتواند به همان راههایی که فلوئور آرایش الکترونی خود را به آرایش الکترونی گاز بیاثر رساند، آرایش الکترونی خود را کامل کند. یکی از راههای رسیدن به آرایش الکترونی گاز بیاثر آن است که با یک اتم هیدروژن دیگر پیوند برقرار کند و مولکول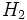 O را پدید آورد.
O را پدید آورد.
پیوند داتیو
اتم نیتروژن با سه اتم هیدروژن ، پیوند کووالانسی معمولی تشکیل میدهد و به آرایش الکترونی گاز بیاثر میرسد. پس از این عمل ، برای نیتروژن یک جفت الکترون غیر پیوندی باقی میماند که میتواند آن را بصورت داتیو در اختیار اتمهایی که به آن نیاز دارند، قرار دهد. از سوی دیگر ، اتم هیدروژن که یک اتم الکترون در اوربیتال 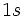 آن موجود است، هر گاه این الکترون را از دست بدهد، به یون
آن موجود است، هر گاه این الکترون را از دست بدهد، به یون  تبدیل میشود که اوربیتال
تبدیل میشود که اوربیتال 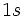 آن خالی است.
آن خالی است.
حال هرگاه این یون به مولکول آمونیاک نزدیک شود، با آن پیوند داتیو برقرار میکند و خود را به آرایش الکترونی گاز بیاثر میرساند:  این مجموعه که یون آمونیوم نامیده میشود، در بسیاری از ترکیبات مانند کلرید آمونیوم
این مجموعه که یون آمونیوم نامیده میشود، در بسیاری از ترکیبات مانند کلرید آمونیوم 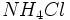 و هیدروکسید آمونیوم
و هیدروکسید آمونیوم  وجود دارد.
وجود دارد.
اندازه گیریهای انجام شده نشان میدهد که انرژی و طول هر چهار پیوند نیتروژن _ هیدروژن در یون آمونیوم کاملا یکسان است. این امر منطقی نیز به نظر میرسد، زیرا پیوند داتیو نیز مانند پیوند کووالانسی معمولی یک جفت الکترون است که بین هسته اتم نیتروژن و هسته اتم هیدروژن قرار گرفته است.
هچنین  میتواند با یون
میتواند با یون 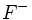 یون
یون  تشکیل دهد که در آن هر چهار پیوند از نظر طول و انرژی یکسان هستند. کلرید آلومینیوم نیز با یون
تشکیل دهد که در آن هر چهار پیوند از نظر طول و انرژی یکسان هستند. کلرید آلومینیوم نیز با یون 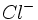 ترکیب میشود و یون
ترکیب میشود و یون  تولید میکند که در آن هر چهار پیوند AL - Cl از نظر طول و انرژی یکسان هستند.
تولید میکند که در آن هر چهار پیوند AL - Cl از نظر طول و انرژی یکسان هستند.
پیوند الکترووالانسی (یونی)
در اتم لیتیم ، 2 الکترون وجود دارد که یک الکترون ، در لایه والانس آن قرار دارد. به هنگام تشکیل پیوند ، چون این اتم در دومین سطح انرژی دارای جفت الکترون غیر پیوندی نیست و تفاوت سطح انرژی اول و دوم نیز بسیار زیاد است، نمیتواند الکترون خود را برانگیخته کند. بنابراین در خارجیترین سطح انرژی ، تنها یک الکترون خواهد داشت. هرگاه این اتم بخواهد پیوند کووالانسی تشکیل دهد، باید یک اتم تک الکترونی دیگر مانند فلوئور پیوند تشکیل دهد و  را تولید کند.
را تولید کند.
واقعیت آن است که از پیوند بین لیتیم و فلوئور ، فلورید لیتیم  پدید میآید، ولی هرگاه بخواهیم این دو اتم را از نظر آرایش الکترونی بررسی کنیم، مشاهده خواهیم کرد که اتم فلوئور با اشتراک گذاشتن الکترون ، ممکن است به آرایش الکترونی گاز بیاثر برسد، ولی لیتیم آرایش الکترونی گاز بیاثر پیدا نکرده است.
پدید میآید، ولی هرگاه بخواهیم این دو اتم را از نظر آرایش الکترونی بررسی کنیم، مشاهده خواهیم کرد که اتم فلوئور با اشتراک گذاشتن الکترون ، ممکن است به آرایش الکترونی گاز بیاثر برسد، ولی لیتیم آرایش الکترونی گاز بیاثر پیدا نکرده است.
لیتیم هر گاه بخواهد به آرایش الکترونی گاز بیاثر بعد از خود برسد، باید روی هم رفته هفت الکترون بگیرد که اگر بخواهد این هفت الکترون را با پیوند کووالانسی بدست آورد، خود نیز باید هفت الکترون در خارجیترین سطح انرژی خود داشته باشد که این کار به هیچ وجه امکان پذیر نیست.
ولی هر گاه این عنصر بخواهد آرایش الکترونی گاز بیاثر قبل خود را پیدا کند، کافی است که یک الکترون موجود در اوربیتال 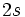 خود را از دست بدهد تا آرایش الکترونی آن به صورت
خود را از دست بدهد تا آرایش الکترونی آن به صورت 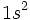 در آید و آرایش الکترونی گاز بیاثر هلیم پیدا کند. یعنی اتم لیتیم به یون
در آید و آرایش الکترونی گاز بیاثر هلیم پیدا کند. یعنی اتم لیتیم به یون  تبدیل میشود و به آرایش گاز هلیم میرسد.
تبدیل میشود و به آرایش گاز هلیم میرسد.
اتم فلوئور نیز میتواند با گرفتن یک الکترون و تبدیل شدن به یون 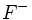 خود را به آرایش الکترونی گاز بی اثر نئون برساند. یعنی به هنگام تشکیل پیوند بین لیتیم و فلوئور ، لیتیم یک الکترون به فلوئور میدهد و با این عمل هر دو به آرایش الکترونی گاز بیاثر میرسند. به این ترتیب اتم فلوئور به یون منفی (آنیون) و اتم لیتیم به یون مثبت (کاتیون) تبدیل میشود. این نوع پیوند را پیوند الکترووالانسی یا یونی مینامند که بین یک فلز و یک غیرفلز رخ میدهد.
خود را به آرایش الکترونی گاز بی اثر نئون برساند. یعنی به هنگام تشکیل پیوند بین لیتیم و فلوئور ، لیتیم یک الکترون به فلوئور میدهد و با این عمل هر دو به آرایش الکترونی گاز بیاثر میرسند. به این ترتیب اتم فلوئور به یون منفی (آنیون) و اتم لیتیم به یون مثبت (کاتیون) تبدیل میشود. این نوع پیوند را پیوند الکترووالانسی یا یونی مینامند که بین یک فلز و یک غیرفلز رخ میدهد.
برچسبها: آرایش الکترونی عناصر, آنیون و کاتیون, پیوند شیمیایی و انواع آن
 که برای رسیدن به آرایش الکترونی گاز بی اثر به دو یا چند الکترون نیاز دارند و یا مولکولهایی مثل
که برای رسیدن به آرایش الکترونی گاز بی اثر به دو یا چند الکترون نیاز دارند و یا مولکولهایی مثل  که در آنها اتم مرکزی در آخرین لایه ، اوربیتال خالی دارد و برای رسیدن به آرایش گاز بی اثر به الکترون محتاج است و در واکنشها به نقاطی متمایل میشوند که دارای الکترون باشند، ذرات الکترون دوستیا الکتروفیل گفته میشود.
که در آنها اتم مرکزی در آخرین لایه ، اوربیتال خالی دارد و برای رسیدن به آرایش گاز بی اثر به الکترون محتاج است و در واکنشها به نقاطی متمایل میشوند که دارای الکترون باشند، ذرات الکترون دوستیا الکتروفیل گفته میشود.ذراتی مثل
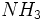 که در آنها اتم مرکزی دارای جفت الکتورن غیر پیوندی بوده و در صورت لزوم میتوانند جفت الکتورن خود را در اختیار اتم دیگر بگذارند و پیوند داتیو برقرار نمایند و در واکنشها به سوی نقاطی که دارای بار مثبت هستند، متمایل شوند، ذرات هسته دوست یا مثبت دوست یا نوکلئوفیل نامیده میشوند.
که در آنها اتم مرکزی دارای جفت الکتورن غیر پیوندی بوده و در صورت لزوم میتوانند جفت الکتورن خود را در اختیار اتم دیگر بگذارند و پیوند داتیو برقرار نمایند و در واکنشها به سوی نقاطی که دارای بار مثبت هستند، متمایل شوند، ذرات هسته دوست یا مثبت دوست یا نوکلئوفیل نامیده میشوند.به این ترتیب تمام یونهای مثبت و مولکولهایی که اتم مرکزی آنها هنوز از نظر آرایش الکترونی شبیه گاز بی اثر نشده است، الکتروفیل هستند و تمام یونهای منفی و مولکولهایی که اتم مرکزی آنها دارای حداقل یک جفت الکترون غیر پیوندی است، نوکلئوفیل میباشند. الکتروفیلها مثل
 ،
، 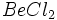 ،
، 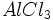 ،
،  ،
، 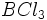 و ... ، نوکلئوفیلها مثل
و ... ، نوکلئوفیلها مثل 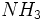 ،
، 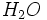 ، آمینها و الکلها و ... .
، آمینها و الکلها و ... .برچسبها: الکتروفیل, نوکلئوفیل, شیمی الی, شیمی تجزیه
