 که برای رسیدن به آرایش الکترونی گاز بی اثر به دو یا چند الکترون نیاز دارند و یا مولکولهایی مثل
که برای رسیدن به آرایش الکترونی گاز بی اثر به دو یا چند الکترون نیاز دارند و یا مولکولهایی مثل  که در آنها اتم مرکزی در آخرین لایه ، اوربیتال خالی دارد و برای رسیدن به آرایش گاز بی اثر به الکترون محتاج است و در واکنشها به نقاطی متمایل میشوند که دارای الکترون باشند، ذرات الکترون دوستیا الکتروفیل گفته میشود.
که در آنها اتم مرکزی در آخرین لایه ، اوربیتال خالی دارد و برای رسیدن به آرایش گاز بی اثر به الکترون محتاج است و در واکنشها به نقاطی متمایل میشوند که دارای الکترون باشند، ذرات الکترون دوستیا الکتروفیل گفته میشود.ذراتی مثل
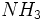 که در آنها اتم مرکزی دارای جفت الکتورن غیر پیوندی بوده و در صورت لزوم میتوانند جفت الکتورن خود را در اختیار اتم دیگر بگذارند و پیوند داتیو برقرار نمایند و در واکنشها به سوی نقاطی که دارای بار مثبت هستند، متمایل شوند، ذرات هسته دوست یا مثبت دوست یا نوکلئوفیل نامیده میشوند.
که در آنها اتم مرکزی دارای جفت الکتورن غیر پیوندی بوده و در صورت لزوم میتوانند جفت الکتورن خود را در اختیار اتم دیگر بگذارند و پیوند داتیو برقرار نمایند و در واکنشها به سوی نقاطی که دارای بار مثبت هستند، متمایل شوند، ذرات هسته دوست یا مثبت دوست یا نوکلئوفیل نامیده میشوند.به این ترتیب تمام یونهای مثبت و مولکولهایی که اتم مرکزی آنها هنوز از نظر آرایش الکترونی شبیه گاز بی اثر نشده است، الکتروفیل هستند و تمام یونهای منفی و مولکولهایی که اتم مرکزی آنها دارای حداقل یک جفت الکترون غیر پیوندی است، نوکلئوفیل میباشند. الکتروفیلها مثل
 ،
، 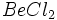 ،
، 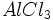 ،
،  ،
، 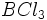 و ... ، نوکلئوفیلها مثل
و ... ، نوکلئوفیلها مثل 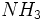 ،
، 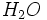 ، آمینها و الکلها و ... .
، آمینها و الکلها و ... .برچسبها: الکتروفیل, نوکلئوفیل, شیمی الی, شیمی تجزیه
1- تیل چیست و استفاده از آن در این آزمایش چه مزیتی نسبت به بشر دارد؟
*وسیله ی ساده ای است که به سهولت قابل دسترسی است.لوله ی تیل به نحوی طراحی شده است،
که وقتی در آن روغن میریزیم و لوله را گرم میکنیم در آن تبادل گرمایی صورت میگیرد به نحوی که توزیع دما،
در سراسر روغن داخل لوله یکنواخت می شود.
2- چرا نمیتوان از نمونه ای که یکبار دمای ذوب آن اندازه گیری شده است برای
اندازه گیری مجدد دمای ذوب استفاده کرد؟
*وقتی یک جسم جامد به دمای ذوب خود برسد، ساختار اولیه اش تغییر میکند؛
در نتیجه در مرتبه دوم دمای ذوب متفاوتی از دمای ذوب اولیه خواهیم داشت.
3- چرا بجای نقطه ذوب، اصطلاح دمای ذوب را بکار میبریم؟
*در اکثر مواد بجای نقطه ذوب، از گستره دمایی که در آن ماده شروع به ذوب شدن میکند تا دمایی که بطور کامل
ذوب میشود را مد نظر قرار میدهند؛ به همین دلیل اصطلاح دمای ذوب بکار میرود.
4- یک دانشجو دمای ذوب ماده دارای ناخالصی شن را 130-118 درجه سانتی گراد بدست آورد، در حالیکه
دمای ذوب ماده خالص 123-121 درجه سانتی گراد گزارش شده است! این پدیده را چگونه توجیح میکنید؟
*ناخالصی موجب زیاد شدن گستره دمای ذوب میشود؛ تبلور مجدد یک ترکیب ناخالص موجب خالص شدن آن
و در نتیجه کاهش گستره دمای ذوب میگردد.
آزمایش دمای جوش
1- علت خروج حباب ها از لوله موئین در روش میکرو چیست؟
*با افزایش دما، کم کم مایع به فاز بخار میرود و همین امر سبب افزایش فشار بخار روی سطح مایع میگردد؛
در نتیجه فشار وارد بر سطح مایع بیشتر از فشار گاز درون لوله موئین خواهد شد، به همین دلیل بتدریج هوای
درون لوله موئین با ایجاد حباب خارج میشود.
2- چرا پس از خروج مکرر حباب هیتر را خاموش میکنیم؟
*چون این حالت نشانگر محلول ابر گرم شده است، یعنی دمای ماده بیشتر از دمای جوش است بنابراین
هیتر را خاموش میکنیم تا دما پائین بیاید و بتوانیم دمای جوش را اندازه گیری کینم.
- محلول ابر گرم شده را تعریف کنید؟
*محلولی است که در آن، فشار کمتر از فشار جو و دما بیشتر از دمای جوش است اما ماده هنوز نجوشیده است.
آزمایش تبلور مجدد
1- چرا به این روش، تبلور مجدد میگویند؟
*وقتی ماده به صورت جامد باشد، سپس آن را در حلالی حل کرده و مجددا آن را به صورت بلور رسوب گیری کنند،
تبلور مجدد مینامند.
1- تبلور با رسوب گیری چه تفاوت هایی دارد؟
*تبلور فرآیندی کند و انتخابی است، اما رسوب گیری سریع و غیر گزینشی است.
2- چرا برای تبلور باید از حلالی استفاده کرد که دمای جوش آن کوچکتر از دمای
ذوب ماده خالص باشد؟
*در غیر اینصورت ماده متبلور، مجددا ذوب شده و ایجاد امولسیون کرده و در نهایت
روغنی شدن رخ میدهد.
3- چرا برای بدست آوردن بلور خالص در مرحله آخر قیف بوخنر استفاده میشود؟
*تبلور فرآیندی کند است؛ از قیف بوخنر برای تسریع عمل تبلور استفاده میشود.
آزمایش استخراج کافئین از چای
1- چرا از آب به عنوان حلا اول استفاده شده است؟
*آب دمای جوش بالایی دارد و باعث استخراج کافئین از نسوج گیاهی میود.
2- چرا از حلال دومی، مانند CH2 CL2 و... استفاده میشود؟
*تا کافئین را که یک ترکیب آلی ست، در خورد حل کرده و از طرف دیگر به علت
دمای جوش پائین تبخیر آن نیز راحت تر صورت گیرد.
3-برای استخراج کافئین، اضافه کردن نمک Na2 CO3 مناسب تر است یا Na CL؟ و چرا؟
Na CL؛ زیرا Na2 CO3 یک گونه بازی است و کافئین هم حالت بازی دارد، و از آنجا که دو گونه هم سان
از یکدیگر فرار میکنند، Na CL برای این کار بهتر است.
آزمایش تقطیر
1- چرا مایع داخل بالن باید بین یک سوم تا دو سوم حجم بالن باشد؟
*چون اگر کم باشد، فشار کافی برای تقطیر فراهم نمیشود، و اگر زیاد باشد
سر ریز میشود.
2-چرا بهتر است، که قبل از پایان یافتن همه مایع داخل بالت تقطیر را قطع کرد؟
*چون مواد تـــه ظرف غیر فرارند و خارج نمیشوند و باقی مانده به تـــه ظرف میچسبد.
3- چرا مایعات تقطیر شده قبل از ثبات دمایی را دور میریزیم و این مواد چه میباشند؟
*چون این مایعات دارای ناخالصی هستند و ممکن است غیر فرار باشند.
4- چرا در تقطیر از سیستم کاملا بسته استفاده نمیشود؟
*چون باعث انفجار میگردد.
5-علت اضافه کردن سنگ جوش به بالن چیست؟
*به منظور توزیع یکنواخت گرما و جلوگیری از پریدن مایع است.
6- آزئوتروپ چیست؟
*به دو ماده که باهم در یک دما بجوش می آیند، آزئوتروپ میگویند. آزئوتروپ به
معنای همسان جوش یا هم جوش میباشد؛ به این معنی که وقتی محلول به نقطه آزئوتروپ میرسد در فشار ثابت و غلظت ثابت آنقدر در نقطه آزئوتروپ میماند
تا به بخار هم غلظت با خود تبدیل شود.برچسبها: پاسخ, آزمایشگاه آلی
دانلود جلد اول دوم و سوم اینجا
دانلود پاسخ سوالات کتاب از اینجا
برچسبها: شیمی آلی, آزمایشگاه شیمی آلی
نيتراته کردن استانيليد و استيلاسيون:
زمانيکه كه نيترات يا سولفات آنيلين در درجه حرارت پايين توسط نيتريك اسيد و سولفوريك اسيد نيتره گردند، محصول داراي حدود 60% متانيتروآنيلين و 38% پارانيتروآنيلين است، كه همراه با آن مقدار كمي ارتو نيترو آنيلين نيز وجود دارد. بعلت اكسيدشدن مقداري از آنيلين بهره بالا نميباشد.
مسلما نيترو آنيلين محصول اصلي است زيرا که گروه با بار "مثبت" "NH3-" خاصيت كشندگي الكترون قوي دارد. در ضمن اين گروه شديداً باعث غيرفعال شدن جايگاههاي ارتو و پارا ميگردد.مقدار قابل ملاحظهاي از پارانيتروآنيلين به وجود ميآيد.
نسبت مشاهده شده براي پارا/متا ميزان اثر سوق دهندگي گروه –NH3+ را ارائه ميدهد. وسعت نيتراسيون پارا با قراردادن گروههاي متيل پي در پي روي اتم ازت كاهش مييابد، در C6H5-N(CH3)+3 منجر به ايجاد 89% متا و 11% مشتق پارانيترو ميگردد.
براي كاهش اكسيداسيون و جلوگيري از اثر سوق دهندگي متا در نمك ايجادي، قبل از نيتراسيون تركيب، آمين آروماتيك را به مشتق استيل تبديل مينمايند. متعاقباً گروه آمين را توسط هيدروليز با محلول آلي اسيدباز برميدارند.
بدين ترتيب آنيلين به استانيليد تبديل شده تحت نيتراسيون معمولي تقريباً تمام آن به پارا نيترواستانيليد تبديل ميگردد، كه در اثر هيدروليز آن پارا نيتروآنيلين بدست ميآيد.
از آنجايي كه فقط مقدار جزئي از ارتو نيترواستانيليد از نيتراسيون حاصل ميگردد، روش غيرمستقيم در يك سري واكنشها براي ايجاد ارتو بعنوان محصول اصلي بكار گرفته ميشود. انيلين به اسيد سولفانيليكي تبديل ميشود كه در آن موقعيت پارا توسط گروه So3H مسدود شده است. نيتراسيون اسيدسولفانيليك توليد -4 آمينو -3 نيتروبنزن سولفونيك اسيد مينمايد، هيدروليز تركيب اخير كه توسط جوشاندن آن با اسيدسولفوريك 60% صورت ميگيرد، حذف گروه So3H را باعث شده و ارتو نيترو آنيلين را با حالات خصوصي بالا در اختيار ميگذارد.
هر 3 نيتروآنيلين بازهاي بينهايت ضعيفي ميباشند، اما از نظر قدرت اسيدي با يكديگر تفاوت قابل ملاحظهاي دارند:
ارتو > پارا > متا
مخلوط نيتروآنيلينها را ميتوان از حل نمودن آنها در اسيدآبي قوي و سپس رسوبگيري پيدر پي، ايزومرهاي ارتو، متا و پارا كه توسط خنثيسازي آنها با آمونياك رقيق انجام ميشود، جدا نمود.
مواد لازم: پارانيترو استانيليد، اسيد سولفوريک غليظ،سديم هيدروکسيد 10%، اتانول
وسايل لازم: ارلن ماير در چند سايز مختلف، کاغذ صافي، حمام آب و يخ، هم زن شيشهاي، قيف، ترازوي ديجيتالي، شيشه ساعت، قيف بوخنر،استوانه مدرج
فرمول واکنش :

![]()
خطای آزمایش:
چون در حین افزایش محلول سدیم هیدروکسید مخلوط گرم می شود باید به خوبی همزده شود.
نتیجه گیری:
پارا نيترو استانيليد از طريق هيدروليز در محيط اسيدي داستيله مي شود و ايجاد پارا نيترو
آنيلين مي كند. بدين ترتيب گروه استيل كه براي محافظت گروه عاملي آمين بكار رفته بود
براحتي خارج مي شود .
1-در تهیه P-نیترو آنیلین چرا به جای نیترو دار کردن آنیلین استانیلید نیترو دار و هیدرولیز می شود؟
زیرا در استانیلید گروه آمینو بین دو گروه پذیرنده الکترون یعنی حلقه بنزن و گروه کربونیل قرار دارد به همین دلیل خاصیت بازی ندارد و با اسیدها نمک تولید نمی کند.
2- اگر P-نیترواستانیلید در محلول های اسیدی هیدرولیز می شودچرا هیدرولیز در نیترو دار کردن با مخلوط HNO3 و H2SO4 رخ نمی دهد؟
C6H5-NH(C=O)CH3 استانیلید می باشد که در آن گروه NHCOCH3 بر روی حلقه ی آروماتیکی وجود دارد. حال چنانچه بخواهیم یک گروه دیگر بر روی حلقه قرار دهیم، این گروه می تواند موقعیتهای ارتو، متا و پارا را اشغال نماید. یعنی گروه جدید همسایه ی گروه قبلی باشد (ارتو) و یا یک کربن از آن فاصله داشته باشد(متا) و یا دو کربن فاصله داشته باشد و در دورترین فاصله ی ممکن قرار گیرد (پارا).
استانیلید دارای نقطه ذوب 113 تا 115 درجه ی سانتیگراد و نقطه جوش 304 درجه ی سانتیگراد می باشد.
ارتو
و پارا نیترواستانیلید بوسیله ی واکنش استانیلید با مخلوطی از نیتریک اسید
و سولفوریک اسید بدست می آید. زیرا گروه نخست یعنی NHCOCH3 گروه حجیمی
است، فرم پارا که در آن دو گروه فوق و نیترو از هم فاصله ی بیشتری دارند،
پایدارتر بوده و قسمت بیشتر محصول را به خود اختصاص می دهد. اما جدا کردن
ایزومرهای پارا و ارتو از طریق تقطیر جز به جز ممکن است، زیرا ابن دو ترکیب
در نقطه ی جوش متفاوت هستند.
واکنش استانیلید با نیتریک اسید غلیظ سبب
تولید پارانیترواستانیلید می شود. برای بالا بردن بازده می توان از نسبت 3
به 1 از سولفوریک اسید و نیتریک اسید استفاده نمود. چون این واکنش گرمازا
است، باید افزایش استانیلید به اسید نیتریک غلیظ بسیار آهسته و همراه با
سردکردن محیط واکنش صورت گیرد.
دکانتور یا قیف جداکننده ، وسیله ای است
که به کمک آن می توان دو فاز آبی و آلی را از هم جدا نمود. این وسیله در
قسمت انتها دارای یک شیر است که با باز کردن آن، لایه ی زیرین به راحتی از
لایه ی بالایی جدا می شود.
پلیمر شدن زنجیری رادیکال آزاد ، را می توان از مهمترین روشهای صنعتی تهیه پلیمرها به حساب آورد ، پلی اتیلن ، پلی استیرن یا پلی استایرن و پلی وینیل کلرید ، پلیمرهای مهم اقتصادی هستند که توسط این فرایند تولید می شوند . پلیمرهایی از قبیل ؛ پلی متیل متا کریلات ، پلی وینیل استات و پلی اکریلونیتریل را نیز می توان با چنین فرایندهایی تهیه نمود .
موضع انتشار یک رادیکال آزاد یا به عبارتی یک الکترون جفت نشده ، روی آخرین اتم کربن زنجیر در حال رشد می باشد ، پلیمر شدن رادیکال آزاد شامل مراحل رشد زیادی است ، که در آنها موضع رادیکال مجدداً روی آخرین واحد جدید زنجیر تشکیل خواهد شد .
تهیه پلی استیرن یا پلی استایرن نیز توسط پلیمریزاسیون زنجیری رادیکال آزاد انجام می شود .

از مونومرهایی که برای پلیمر شدن رادیکال آزاد بسیار مناسب هستند ، می توان به استیرن و استخلافهای استیرنی ، دی ان ها ، وینیل پیریدین ، الکیل آکریلات و متاکریلات ، اکریلونیتریل ، وینیل کلرید و وینیل استات اشاره نمود .
مکانیسم پلیمر شدن ( پلیمریزاسیون ) رادیکال آزاد :
این مبحث به پلیمر شدن یک پلیمر وینیلی با آغازگر متقارنی مانند : آزوبیس ایزوبوتیرو نیتریل (AIBN) یا دی بنزوئیل پروکسید که در محیط همگن انجام می گیرد اختصاص دارد .
مکانیسم پلیمر شدن رادیکال آزاد شامل سه مرحله است : آغاز – انتشار – پایان
آغاز :
مولکول مونومر در واکنش آغاز به وسیله رادیکال آزاد اولیه حاصل از ، آغازگر ، مورد حمله قرار می گیرد . این فرایند شامل دو واکنش است : تجزیه آغازگر به رادیکالهای اولیه و واکنش شروع حقیقی .
در شکل زیر ساختار بنزوئیل پروکسید و واکنش تجزیه آغازگر به رادیکالهای اولیه را مشاهده می کنید :

در شکل زیر مکانیسم واکنش شروع پلیمر شدن رادیکال آزاد را مشاهده می کنید :

انتشار :
واکنش انتشار ، برای تشکیل هر زنجیر هزاران بار تکرار می گردد . در شکل زیر مکانیسم واکنش انتشار را مشاهده می کنید :

پایان :
رادیکالهای در حال رشد می توانند به دو صورت مختلف با هم واکنش دهند :
به وسیله ترکیب مجدد ، یک پیوند جور قطبی با جفت شدن الکترونهای منفرد مراکز رادیکال های آزاد ، که منجر به تشکیل دو زنجیر می شود .
به وسیله تسهیم نا مناسب ، که در طی آن یک اتم هیدروژن از یک زنجیر به زنجیر دیگر منتقل شده و دو مولکول پلیمری مرده را بوجود می آورد . که یکی از آنها حامل یک پیوند دوتایی در انتهای زنجیر خود خواهد بود .
در هر دو مورد ، واکنشها شامل تخریب متقابل رادیکالی هستند .
پلیمریزاسیون رادیکالی را می توان با استفاده از چهار روش زیر انجام داد :
الف) پلیمریزاسیون توده ب) پلیمریزاسیون محلول ج) پلیمریزاسیون تعلیقی د) پلیمریزاسیون امولسیون
روش کار تهیه پلی استیرن :
الف ) تهیه پلی استیرن با استفاده از روش پلیمریزاسیون توده :
3 میلی لیتر استیرن را در یک لوله آزمایش بریزید ، سپس به اندازه نوک اسپاتول ، بنزوئیل پروکسید به عنوان آغازگر به آن اضافه کنید . لوله آزمایش را با یک درپوش ببندید ، و به آرامی آن را تکان دهید ، تا آغازگر حل شود . سپس درپوش را بردارید و لوله را درون یک حمام آب جوش قرار دهید . پس از حدود 1 الی 5/1 ساعت محتویات لوله آزمایش تبدیل به مایع ویسکوزی می شود . پلیمر را می توان در صورت لزوم در مقدار کمی تولوئن حل کرد . حال اگر این محلول را درون یک ارلن که محتوی 30میلی لیتر متانول سرد است ، بریزید ، پلی استیرن به صورت پلیمر جامد سفید رنگی رسوب خواهد کرد ، که می توان آن را بوسیله صاف کردن یا دکانت کردن جدا کرده و با متانول شستشو داد .
ب ) تهیه پلی استیرن با استفاده از روش پلیمریزاسیون محلول :
بداخل بالن 100 میلی لیتری خشک و تمیز و مجهز به مبرد رفلاکس ، محلول 3 میلی لیتر استیرن تازه تقطیر شده در 10 میلی لیتر تولوئن را بریزید . سپس 5/1 میلی لیتر از محلول ، 08/0 گرم بنزوئیل پروکسید در 5 میلی لیتر تولوئن را به محتویات داخل بالن اضافه کنید . با انداختن سنگ جوش عمل رفلاکس ( بازروانی ) را به آرامی به مدت 5/1 ساعت انجام دهید . بعد از این مدت منبع گرمایی را حذف کرده و اجازه دهید بالن سرد شود . محتویات بالن را به داخل ارلن محتوی 100 میلی لیتر متانول سرد بریزید . در این حالت پلی استیرن به صورت پلیمر جامد سفید رنگی رسوب خواهد کرد ، این رسوبات را بوسیله صاف کردن یا دکانت کردن از محلول جدا کرده و با متانول شستشو دهید .
در شکل زیر ساختار سه بعدی یا فضایی پلی استیرن را مشاهده می کنید :


