اگر گروههای عاملی روی حلقه قرار بگیرند، بر واکنش پذیری حلقه اثر خواهند گذاشت. واکنش پذیری عوامل متصل به حلقه نیز بوسیله بخش آروماتیک تحتتاثیر قرار میگیرد.
مشتقات بنزن با فشار بالا و نقطه جوش پایین هستند که با افزایش وزن مولکولی افزایش می یابد . این حلال دارای دانسیته بخار بالا هستند . بیشتر این ترکیبات به عنوان مواد شمیایی اولیه یا واسطه در ترکیبات دیگر بکار می روند. حلالهای الی همچنین در هزاران صنعت وشغل مثل :تولید رنگ ،رزین ومواد دارویی ،چاپ ، سریش و چسبها و ساخت لاستیک و… بکار می رود.
ترکیبات اروماتیک معمول استفاده شده شامل تولوئن ،بنزن ،زایلن ،استیرن ،اتیل بنزن ،مونوکلروبنزن (MCB ) وتری متیل بنزن می باشد.
بیشتر حلالهای اروماتیک تجاری نقطه جوشی دارند که خیلی کمتر از صفر درجه و بشتر از 200 درجه سانتیگراد نمی باشد .اگر نقطه جوش یک حلال خیلی بالاوفشار بخار آن خیلی کم باشد جداسازی حلال از موادی که برای حل کردن استفاده می شود بسیار دشوار خواهد بود.بنابراین بسیاری از حلالهای الی در دمای اتاق مایع هستند . حلالهای الی بوسیله خصوصیت غیر قطبی وحلالیت بالا در چربی توصیف می شوند . این حلالها به فراوانی در مخلوطهایی در محیطهای شغلی مثل ترکیبات تولوئن ، بنزن ، استیرن ،اتیل بنزن ، تری متیل بنزن و زایلن استفاده شده است . نفتالن ، اگر چه یک ترکیب اروماتیک است حلال نیست ، جامدی کریستالی ، سفید رنگ دافع بید و با فراریت بالا می باشد . حلالهای اروماتیک به اسانی از تصفیه نفت خام و زغال مشتق می شود وقتی زغال در فقدان هوا گرم می شود به ترکیبات فراری شامل گاز زغال وقطران زغال شکسته می شود . باقیمانده این پروسه کک نامیده می شود . تقطیر قطران زغال منجر به تولید ترکیباتی مثل تولوئن ،بنزن ،زایلن ، فنول ها ، کروزول ، نفتالن می شود.ترکیبات اروماتیک همچنین می تواند توسط فرایند های کاتالیکی که در ان هیدروکربن های الیفاتیک در دماهای بالا وفشار بالا برای دهیدروژنه کردن ترکیبات وشکل گیری ساختارهای حلقوی هیدروکربن های اروماتیک بکار می رود ایجاد می شوند .
Azoxybenzene and Aluminum Chloride
Aromatic Compounds

Procedure
Place 0.5 mL or 0.4 g of the dry compound in a clean, dry test tube; add one crystal of azoxybenzene and about 25 mg of anhydrous aluminum chloride. Note the color. If no color is produced immediately, warm the mixture for a few minutes. Wait for up to 30 min to observe any color change. If the hydrocarbon is a solid, a solution of 0.5 g of it in 2 mL of dry carbon disulfide may be used.
Positive Test
Formation of 4-arylazobenzene and aluminum chloride complex is a positive test.
Complications
Many oxygen-containing functionalities interfere with this test and produce confusing color changes
Chloroform and Aluminum Chloride
Aromatic Compounds

Procedure
To 2 mL of dry chloroform in a test tube add 0.1 mL or 0.1 g of the unknown compound. Mix thoroughly, and incline the test tube so as to moisten the wall. Then add 0.5-1.0 g of anhydrous aluminum chloride so that some of the powder strikes the side of the test tube. Note the color of the powder on the side, as well as the solution. Discussion. The colors produced by the reaction of aromatic compounds with chloroform and aluminum chloride are quite characteristic. Aliphatic compounds, which are insoluble in sulfuric acid, give no color or only a very light yellow. Typical colors produced are the following.
Positive Test
Formation of a colored carbocation is a positive test.
| Compound | Color |
| benzene and its homologs | orange to red |
| aryl halides | orange to red |
| naphthalene | blue |
| biphenyl | purple |
| phenanthrene | purple |
| anthracene | green |
Complications
Aromatic esters, ketones, amines, and other oxygen- or nitrogen-containing compounds may also give blue or green colors.
Reaction of Bromine with Benzene, Phenol, and Toluene
Three test tubes contain bromine. Benzene is added to the first tube, phenol to the second, and toluene to the third tube. The red color of the bromine vapor disappears from the second tube containing the phenol. pH paper indicates that hydrogen bromide was produced in this reaction.
Discussion
Bromine is shown in each of three test tubes. Benzene is added to the first tube, phenol to the second, and toluene to the third tube. The red color of the bromine vapor disappears from the second tube containing the phenol. When the vapor in this tube is tested with pH paper, the red color indicates the presence of an acidic gas (hydrogen bromide). Benzene and toluene do not react with bromine in the absence of a catalyst. Phenol is more reactive due to the presence of an electron donating hydroxyl group and reacts with bromine by a substitution reaction forming hydrogen bromide gas.
Fuming Sulfuric Acid
Aromatic Compounds
![]()
Procedure
This test must be done in a hood. Place 0.5 mL of 20% fuming sulfuric acid (hazardous) in a clean, dry test tube, and add 0.25 mL or 0.25 g of the unknown. Shake the mixture vigorously, and allow it to stand for a few minutes.
Positive Test
A positive test for the presence of an aromatic ring is complete dissolution of the unknown, evolution of heat, and minimal charring.
Complications
Caution: Use this reagent with relatively inert compounds only, such as those compounds that do not dissolve in the solubility tests with concentrated sulfuric acid. Compounds for which preliminary tests indicate strongly activating groups (OH, NH2, etc.) may be decomposed violently by fuming sulfuric acid.
Aromatic Substitution Reactions
Aromatic Substitution Reactions Part II
کربن عنصری شیمیائی در جدول تناوبی است، با نشان C و عدد اتمی ۶. کربن عنصری غیر فلزی و فراوان، چهارظرفیتی ودارای سه آلوتروپ میباشد:
الماس (سختترین کانی شناخته شده)
گرافیت(یکی از نرمترین مواد)
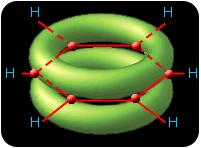
Covalend bound sp1 orbitals are of chemical interest only
فولریت (فولرین ها، مولکولهایی در حد بیلیونیوم متر هستند که در شکل ساده آن، 60 اتم کربن یک لایه گرافیتی با ساختمان 3 بعدی منحنی، شبیه به روروئک (روروئکی که قسمت جلوی آن مانند چوب اسکی خم شده)، تشکیل میدهند .
دوده چراغ از سطوح کوچک گرافیت تشکیل شده. این سطوح بصورت تصادفی توزیع شده، به همین دلیل کل ساختمان آن همسانگرد (ایزوتروپیک) است.
چنین کربنی همسانگرد و مانند شیشه محکم است. لایههای گرافیت آن مانند کتاب مرتب نشده اند، بلکه مانند کاغذ خرد شده میباشند.
الیاف کربن شبیه کربن شیشهای میباشند. تحت مراقبتهای ویژه (کشیدن الیاف آلی و کربنی کردن) میتوان لایههای صاف کربن را در جهت الیاف مرتب کرد. هیچ لایه کربنی در جهت عمود بر محور الیاف قرار نمیگیرد. نتیجه الیافی با استحکام بیشتر از فولاد میباشد . کربن در تمامی جانداران وجود داشته و پایه شیمی آلی را تشکیل میدهد.همچنین این غیرفلز ویژگی جالبی دارد که میتواند با خودش و انواع زیادی از عناصر دیگر پیوند برقرار کند(تشکیل دهنده بیش از ده میلیون ترکیب).در صورت ترکیب با اکسیژن تولید دی اکسید کربن میکند که برای رویش گیاهان، حیاتی میباشد.در صورت ترکیب با هیدروژن ترکیبات مختلفی بنام هیدرو کربنها را بوجود میآورد که به شکل سوختهای فسیلی، در صنعت بسیار بنیادی هستند. وقتی هم با اکسیژن و هم با هیدروژن ترکیب گردد ،گروه زیادی از ترکیبات را از جمله اسیدهای چرب را میسازند که برای حیات و استر، که طعم دهنده بسیاری از میوهها است، ضروری است.ایزوتوپ C-14 به طور متداول در سن یابی پرتوزایشی کاربرد دارد.
ویژگیهای درخور نگرش
کربن به دلایل زیادی قابل توجه است. اشکال مختلف آن شامل یکی از نرمترین (گرافیت) و یکی از سختترین (الماس) مواد شناخته شده توسط انسان میباشد. افزون بر این، کربن میل زیادی به پیوند با اتمهای کوچک دیگر از جمله اتمهای دیگر کربن، داشته و اندازه بسیار کوچک آن امکان پیوندهای متعدد را بوجود میآورد. این خصوصیات باعث شکل گیری ده میلیون ترکیبات کربنی شده است .ترکیبات کربن زیر بنای حیات را در زمین میسازند و چرخه کربن – نیتروژن قسمتی از انرژی تولید شده توسط خورشید و ستارگان دیگر را تأمین میکند.
کربن در اثر مهبانگ (انفجار بزرگ آغازین) حاصل نشده، چون این عنصر برای تولید نیاز به یک برخورد سه مرحلهای ذرات آلفا (هسته اتم هلیم) دارد. جهان در ابتدا گسترش یافت و به چنان به سرعت سرد شد که امکان تولید آن غیر ممکن بود. به هر حال، کربن درون ستارگانی که در رده افقی نمودار H-R قرار دارند، یعنی جائی که ستارگان هسته هلیم را با فرایند سه گانه آلفا به کربن تبدیل میکنند، تولید شد.
کاربردها
کربن بخش بسیار مهمی در تمامی موجودات زنده است و تا آنجا که میدانیم بدون این عنصر زندگی وجود نخواهد داشت(به برتر پنداری کربن مراجعه کنید).عمدهترین کاربرد اقتصادی کربن، فرم هیدروکربنها میباشد که قابل توجهترین آنها سوختهای فسیلی، گاز متان و نفت خام است.نفت خام در صنعت پتروشیمی برای تولید محصولات زیادی از جمله مهمترین آنها بنزین، گازوئیل و نفت سفید بکار میرود که از طریق فرآیند تقطیر در پالایشگاهها بدست میآیند. از نفت خام مواد اولیه بسیاری از مواد مصنوعی، که بسیاری از آنها در مجموع پلاستیک نامیده میشوند، شکل میگیرد.
دیگر کاربردها :
ایزوتوپ C-14 که در 27 فوریه 1930 کشف شد در سن یابی کربن پرتوزا مورد استفاده است.
گرافیت در ترکیب با خاک رس بهعنوان مغز مداد بکار میرود.
الماس جهت تزئین ونیز در متهها و سایر کاربردهایی که سختی آن مورد استفاده است کاربرد د ارد.
برای تولید فولاد، به آهن کربن اضافه میکنند.
کربن در میله کنترل در واکنشگاههای اتمی بکار میرود.
گرافیت به شکل پودر و سفت شده بهعنوان ذغال چوب برای پخت غذا ،در آثار هنری و موارد دیگر مورد استفاده قرار میگیرد.
قرصهای ذغال چوب در پزشکی که به صورت قرص یا پودر وجود دارند برای جذب سم از دستگاه گوارشی مورد استفاده اند.
خصوصیات ساختمانی و شیمیایی فولرن به شکل ریزتیوب کربن، کاربردهای بالقوه امیدوار کنندهای در رشته در حال شکل گیری نانوتکنولوژی ذارد.
تاریخچه
کربن (واژه لاتین carbo به معنی زغال چوب) در دوران پیشاتاریخ کشف شد و برای مردم باستان که آن را از سوختن مواد آلی در اکسیژن ضعیف تولید میکردند، آشنا بود.(تولید [زغال چوب]]).مدت طولانی است که [الماس] بهعنوان مادهای زیبا و کمیاب به حساب مبه منظور مشاهده لینک ها در سایت ثبت نام کنید.آید. فولرن ،آخرین آلوتروپ شناخته شده کربن در دهه 80 بهعنوان محصولات جانبی آزمایشات پرتو مولکولی کشف شدند.
دگرگونهها (آلوتروپها)
نمودار فازی کربن
تاکنون چهار شکل گوناگون از کربن شناخته شده است: غیر متبلور(آمورف)، گرافیت، الماس و فولرن .
کربن در نوع غیر بلورین آن اساسا گرافیت است اما بصورت ساختارهای بزرگ بلورین وجود ندارد.این شکل کربن، بیشتر بصورت پودر است که بخش اصلی موادی مثل ذغال چوب و سیاهی چراغ (دوده) را تشکیل میدهد. در فشار و دمای اتاق کربن به شکل گرافیت پایدارتر است که در آن هر اتم با سه اتم دیگر بصورت حلقههای شش وجهی- درست مثل هیدروکربنهای معطر - به هم متصل شده اند. هردو گونه شناخته شده از گرافیت، آلفا (شش ضلعی) و بتا (منشور شش وجهی که سطوح آن لوزی است) خصوصیات فیزیکی همانند دارند تنها تفاوت آنها در ساختار بلوری آنها میباشد. گرافیتهای طبیعی شامل بیش از 30% نوع بتا هستند در حالیکه گرافیتهای مصنوعی تنها حاوی نوع آلفا میباشند. نوع آلفا از طریق فرآوری مکانیکی میتواند به بتا تبدیل شود و نوع بتا نیز براثر دمای بالای ۱۰۰۰ درجه سانتیگراد دوباره بصورت آلفا بر میگردد.
گرافیت به سبب پراکندگی ابر pi هادی الکتریسیته است. این ماده نرم بوده و ورقههای آن که اغلب بهوسیله اتمهای دیگر تفکیک شده اند، تنها بهوسیله نیروهای وان در والس به هم چسبیدهاند به گونهای که به راحتی یکدیگر را کنار میزنند.
در دما و فشارهای خیلی بالا کربن به صورت الماس پایدار است که در آن هر اتم با چهار اتم دیگر پیوند دارد.الماس ساختار مکعبی همانند سیلسیم و ژرمانیم دارد و (به سبب نیروی پیوندهای کربن – کربن) با نیترید بور همالکترون(BN) در کنارهم بوده و سخت ترین جسم از نظر مقاومت در برابر سایش به شمار میرود. تبدیل الماس به گرافیت در حرارت اتاق به قدری کند است که محسوس نیست. در برخی شرایط کربن به شکل لونسدالیت (lonsdalite) متبلور میشود که مشابه الماس ولی شش ضلعی است. فولرین ساختاری مثل گرافیت دارد اما بجای بخشهای تماما" شش ضلعی، حاوی پنج ضلعیها (یا احتمالا" هفت ضلعیهای) اتمهای کربن نیز میباشند که ورقه را به شکل کره، بیضی یا استوانه بوجود میآورند. ویژگیهایی از فولرین با نام فولرین باکمینستر (buckminsterfullerene) هم نامیده میشوند هنوز بخوبی بررسی نشده اند. اینگونه ساختار را به گونه کوتاه شده، گلولههای باکی (buckyballs) هم نامیده اند. کل نامگان فولرین برگرفته از نام باکمینستر فولر (Buckminster Fuller)، توسعه دهنده گنبد میلهای میباشد که از ساختار گلولههای باکی تقلید کرد.
پیدایش
تقریبا" ده میلیون ترکیبات کربنی که برای دانش شناخته شدهاند وجود دارد که هزاران نوع آنها در فرآیندهای حیاتی و واکنشهای آلی بسیار مهم اقتصادی، ضروری میباشند.این عنصر به مقدار فراوان در خورشید، ستارگان، ستارههای دنباله دار و نیز در جو بیشتر سیارات یافت میشود.بعضی از شهابسنگها حاوی الماسهای میکروسکپی هستند که در زمانیکه منظومه شمسی هنوز یک دیسک گازی شکل بود شکل گرفته اند.کربن به صورت ترکیب با سایر عناصر در جو زمین وجود دارد و در همه گونه آب حل میشود.کربن به همراه مقادیر کمتر کلسیم، منیزیم و آهن، عنصر اصلی سازنده جرم زیادی از سنگ کربنات (سنگ آهک، دولمیت، سنگ مرمر و ...) میباشد. این عنصر در صورت ترکیب با هیدروژن تولید ذغال سنگ، نفت خام و گاز طبیعی میکند که آنها را هیدرو کربن مینامند. گرافیت به مقدار فراوان در نیویورک و تکزاس، امریکا، روسیه، مکزیک، گرینلند و هند یافت میشود. الماس طبیعی در کیمبرلیت معدنی موجود درچینهها یا ستونهای سنگهای آذرین یافت میشوند.بیشترین الماس در افریقا بویژه افریقای جنوبی، نامیبیا، بوتسوانا، جمهوری کنگو و سیرالئون وجود دارد. همچنین کانادا، قسمتهای قطبی روسیه، برزیل و بخشهای غربی و شرقی استرالیا دارای الماس میباشد.
ترکیبات غیر آلی
معروفترین اکسید کربن، دی اکسید کربن (CO2) است که به مقدار کمتری در اتمسفر زمین وجود دارد. این اکسید توسط موجودات زنده، و برخی موارد دیگر تولید شده و مورد استفاده قرار میگیرد. آب مقدار کمی اسید کربنیک تولید میکند اما دی اکسید کربن مانند بیشتر ترکیباتی که دارای پیوندهای ساده چندگانه با اکسیژنهای روی یک کربن هستند، ناپایدار است. به هر حال، از طریق این واسطه، یونهای کربنات با تشدید تثبیت شده، بوجود میآیند. تعدادی از مواد معدنی مهم، کربناتها هستند که معروفترین آنها کلسیت است. دی سولفید کربن، (2 CS)، هم مانند آن میباشد.
اکسیدهای دیگر آن، مونوکسید کربن (CO) و زیراکسید (suboxide) نادر C3O2 هستند.مونوکسید کربن که گازی بی رنگ و بی بو است بهوسیله اکسیده شدن ناقص بوجود میآید.هر یک از این مولکولها دارای یک پیوند سه گانه و نسبتا" قطبی هستند که ناشی از تمایل به یک پیوند دائمی با مولکولهای هموگلوبین میباشد به طوریکه این گاز بسیار سمی است. سیانید (CN-) دارای ساختار و رفتاری بسیار شبیه به یون هالید بوده و نیترید سیانوژن (CN2) نیز به آن مربوط است .
کربن با فلزات قوی، کاربید C- , و یا استیلید C22- ; بوجود میآورد که با متان و استیلن همراه بوده و هر دوی آنها اسیدهای به طور باور نکردنی پائتیک اسید هستند. در کل ،کربن با الکترو نگاتیوی 5/2 به تشکیل پیوندهای کووالانسی تمایل دارد. تعداد کمی از کاربیدها مثل کربوراندوم و Sic، که شبیه الماس میباشند، بصورت شبکههای کوالانسی هستند.
زنجیره کربن
در ساختار اتمی هیدروکربنها، گروهی از اتمهای کربن (اشباع شده با اتمهای هیدروژن) تشکیل یک زنجیره میدهند.روغنهای فرار زتجیرههای کوچک تری دارند.چربیها دارای زنجیرههای بلندتر و پارافینها زنجیرههایی بیاندازه بلندی دارند .
چرخه کربن
فرآیند مداوم ترکیب و آزادسازی کربن و اکسیژن که در آن انرژی و حرارت ذخیره و دفع میشود را چرخه کربن میگویند.فروگشت (کاتابولیسم) + فراگشت (آنابولیسم) = دگرگشت (متابولیسم). (واژهها از فرهنگستان زبان و ادب فارسی). به چرخه کربن مراجعه کنید
ایزوتوپها
اتحادیه بین المللی شیمی کاربردی و محض در سال 1961 ایزوتوپ کربن- 12 را برای اوزان اتمی اتخاذ کرد.کربن- 14 رادیوایزوتوپی است با نیمه عمر 5715 سال و برای تاریخ یابی رادیو کربن چوب، نقاط باستانشناسی و نمونهها کاربرد بسیار زیادی دارد. کربن دارای دو ایزوتوپ پایدار طبیعی میباشد: (C-12(%98.89 و C-13(%1.11) .نسبت این ایزوتوپها در؟ به نسبت الگوی VPDB (Vienna Pee Dee Belemnite from the Peedee Formation of South Carolina). d C-13 در اتمسفر 7 -؟ است است. هنگام فتوسنتز، کربنی که در بافت گیاه تثبیت میشود، به طور قابل ملاحظهای به C-13 موجود در جو بستگی دارد.
دو حالت برای توزیع مقادیر dC-13 در گیاهان خشکی وجود دارد که ناشی از تفاوتهایی است که گیاهان در واکنشهای فتوسنتز بکار میبرند.بیشتر گیاهان خشکی، گیاهان مسیر C3 هستند و دارای ارزشهای dC-13 بوده که بین 24- و 34- قرار دارند(؟).دومین گروه از گیاهان (گیاهان مسیر C4) میباشند که ترکیبی از گیاهان آبی، صحرایی، شوراب زار و مرغزارهای استوایی هستند، و دارای ارزشهای dC-13 بین 6- و 19- میباشند. یک گروه واسطه (CAM plants)، متشکل از جلبک و گلسنگ، دارای ارزشهای dC-13 میباشد که بین 12- و 23-؟ هستند. dC-13 گیاهان و موجودات زنده دادههای سودمندی درباره مواد مغذی و ارتباطات شبکه غذایی ارائه میکند.
هشدارها
ترکیبات کربن گستره وسیعی از آثار سمی دارند.مونوکسید کربن (C O) موجود در اگزوز موتورهای درونسوز و سیانید (CN) که گاهی اوقات در آلودگیهای معدنی وجود دارد برای پستانداران بسیار سمی هستند. بسیاری از ترکیبات دیگر کربن نه تنها سمی نیستند بلکه در واقع برای زیست ضروری میباشند.گازهای آلی مثل اتیلن (H2C=CH2) و اتان و (HCCH)، و متان (CH4) در صورت مخلوط شدن با هوا قابلیت انفجار و اشتعال خطرناکی پیدا میکنند.
