نگاه كلي
شيميدان آلي باتجربه به ندرت واكنش هايي را مي يابد كه فقط محصول (يا محصولات)مورد نظرش را توليد كند.علت اين عمل آن است كه در مخلوط واكنش همراه با محصول مورد نظر مقادير مختلفي از مواد اوليه تغيير نيافته و حلال ومحصول واكنشهاي جانبي كه همزمان با واكنش اصلي انجام مي شوند وجود دارد.
شيميدان نيروي زيادي را صرف مي كند تا محصول مورد نظر را از چنين ناخالصي هايي جدا كند.هدف از اين تحقيق ارائه روشهاي مهمي است كه شيميدان امروزي جهت تفكيك و تخليص تركيبات آلي به كار برد.
تقطير
روشهاي مختلفي براي جداسازي مواد اجزاي سازنده يك محلول وجود دارد كه يكي از اين روشها فرايند تقطير ميباشد در روش تقطير جداكردن اجزاء يك مخلوط ، از روي اختلاف نقطه جوش آنها انجام ميگيردتقطير ، در واقع ، جداسازي فيزيكي برشهاي نفتي است كه اساس آن ، اختلاف در نقطه جوش هيدروكربنهاي مختلف است. هر چه هيدروكربن سنگينتر باشد، نقطه جوش آن زياد است و هر چه هيدروكربن سبكتر باشد، زودتر خارج ميشود.. تقطير در عمل به دو روش زير انجام ميگيرد. روش اول شامل توليد بخار از طريق جوشاندن يك مخلوط مايع ، سپس ميعان بخار ، بدون اينكه هيچ مايعي مجددا به محفظه تقطير بازگردد. در نتيجه هيچ مايع برگشتي وجود ندارد. در روش دوم قسمتي از بخار مايع شده به دستگاه تقطير باز ميگردد و به صورتي كه اين مايع برگشتي در مجاورت بخاري كه به طرف مبرد ميرود قرار ميگيرد. هر كدام از اين روشها ميتوانند پيوسته يا ناپيوسته باشند.
تقطير، معمولترين روشي است كه براي تخليص مايعات به كار مي رود. دراين عمل مايع را به كمك حرارت تبخير مي كنند و بخار مربوطه را در ظرف جداگانه اي متراكم مي كنند و محصول تقطير را بدست مي آورند. چنانچه ناخالصيهاي موجود در مايع اوليه فرار نباشند، در باقي مانده تقطير به جا مي مانند و تقطير ساده جسم را خالص ميكند. در صورتي كه ناخالصيها فرار باشند، تقطير جزء به جزء مورد احتياج خواهد بود.
چنانچه ناخالصي هاي موجود در مايع اوليه فرار نباشد در باقيمانده تقطير به جا مي ماند و تقطير ساده نمونه را خالص مي كند.در صورتيكه فرار باشند تقطير جز به جز مورد نياز خواهد بود.اگر فقط يك ماده فرار بوده و اختلاف نقطه ي جوش اين ماده با ناخالصي هاي موجود در آن زياد باشد (حدود 30درجه)مي توان براي جدا كردن اين ماده از ناخالصي ها از تقطير ساده استفاده نمود.از تقطير ساده معمولا د جداسازي مخلوط مايعاتي استفاده مي شود كه نقطه يجوشي در محدوده 40تا150درجه دارندزيرا در دماي بالاتر از 150درجه بسياري از تركيبات آلي تجزيه مي شوندودر دماي جوش كمتر از 40درجه مقدار زيادي از مايع در ضمن تقطيرهدر مي رود.
در تقطير مخلوطي ازدو يا چند جسم فشاربخار كل تابعي از فشار بخار هر يك از اجزا و كسر مولي آنه مي باشد. بر اساس قانون رائول فشار بخار جزيي يك تركيب فرار در يك محلول ايده آل با حاصلضرب فشار بخار در كسر مولي آن برابر است.بنابراين در بخار موجود بر سطح دو يا چند جزمحلول فرار ذرات كليه اجزا شركت كننده در محلول يافت مي شود.رابطهي بين فشار بخار كل(Pt)با فشار جزيي (Pi)و كسر مولي اجزا(Xi)به صورت زير است:
Pt=PaXa+PbXb+PcXc+……
نكته:اگر در محلولي شامل دو ماده شيميايي فرار يك جز داراي فشار بخار بيشتري از جز ديگر باشد بخار حاصل از آن در مقايسه با مايع داراي درصد بيشتري از جسم فرارتر خواهد بود.
ظروف معمولي در خلل و شكاف هاي جدار خود داراي بسته ها ي هواي محبوس مي باشند.با ريختن مايع در ظرف محفظه بسته ها از بخار پر مي شود.وقتي كه دماي مايع افزايش مي يابد بخار آنقدر به حالت متراكم باقي مي ماند تا اينكه از فشار بخار روي مايع بيشتر شود.در اين حالت بخار به دام افتاده افزايش حجم پيدا مي كند و به صورت حباب هايي به سطح مايع رسيده و خارج مي گردد. حالت به هم خوردگي حاصل از حباب ها (جوش)حباب هاي هواي بيشتري را به داخل مايع كشانده و فرايند با تشكيل بخار ادامه مي يابد.
با حرارت دادن مايعات درظروف شيشه اي كه داراي سطوحي نسبتا صاف و يكنواخت مي باشند حالت جوش ايجاد نمي شود و اگر درجه حرارت به اندازه كافي افزايش يابد به حالت انفجاري تبخير مي گردند.براي اجتناب از خطرات مربوط به جوشش ناگهاني (به صورت ضربه اي)منبعي براي دميدن حباب ها به درون مايع قبل از حرارت دادن و عمل جوش لازم است. در شرايط معمولي (فشارجو)اين منبع سنگ جوش مي باشد.سنگ جوش دانه هايي حاوي خلل ريز در خود بوده كه در آن مولكولهاي هوا حبس شده اند.با قرار گرفتن اين دانه ها در حلول حباب ها از سطح آنها تشكيل شده واز جوشيدن انفجاري و تاخير در جوش جلوگيري مي نمايد.
در ادامه به معرفي انواع روشهاي تقطير و توضيح اجمالي در ارتباط با آنها پرداخته ايم:
انواع تقطير :
تقطير ساده:
به عنوان مثال هنگاميكه ناخالصي غير فراري مانند شكر به مايع خالصي اضافه مي شود فشار بخار مايع تنزل مي يابد.علت اين عمل آن است كه وجود جز غير فرار به مقدار زيادي غلظت جز اصلي فرار را پايين مي آورد يعني ديگر تمام مولكولهايي كه در سطح مايع موجودند مولكولهاي جسم فرار نيستند و بدين ترتيب قابليت تبخير مايع كم مي شود.نمودار ارائه شده در زير اثر جز غير فرار را در فشار بخار مخلوط نشان مي دهد:
تقطير ساده را مي توان به دوصورت تعريف كرد:1-تقطير ساده غير مداوم2-تقطير ساده مداوم
• تقطير ساده غير مداوم : در اين روش تقطير ، مخلوط حرارت داده ميشود تا بحال جوش درآيد بخارهايي كه تشكيل ميشود غني از جزء سبك مخلوط ميباشد پس از عبور از كندانسورها (ميعان كننده ها) تبديل به مايع شده ، از سيستم تقطير خارج ميگردد. به تدريج كه غلظت جزء سنگين مخلوط در مايع باقي مانده زياد ميشود، نقطه جوش آن بتدريج بالا ميرود. به اين ترتيب ، هر لحظه از عمل تقطير ، تركيب فاز بخار حاصل و مايع باقي مانده تغيير ميكند.
• تقطير ساده مداوم : در اين روش ، مخلوط اوليه (خوراك دستگاه) بطور مداوم با مقدار ثابت در واحد زمان ، در گرم كننده گرم ميشود تا مقداري از آن بصورت بخار درآيد، و به محض ورود در ستون تقطير ، جزء سبك مخلوط بخار از جزء سنگين جدا مي شود و از بالاي ستون تقطير خارج ميگردد و بعد از عبور از كندانسورها ، به صورت مايع در ميآيد جزء سنگين نيز از ته ستون تقطير خارج ميشود. قابل ذكر است كه هميشه جزء سبك مقداري جزء سنگين و جزء سنگين نيز داراي مقداري از جزء سبك است.
نكته:در تقطير يك ماده خالص چنانچه مايع زياده از حد گرم نشوددرجه حرارتي كه در گرماسنج ديده مي شود يعني درجه حرارت دهانه ي خروجي با درجه حرارت مايع جوشان در ظرف تقطير يعني درجه حرارت ظرف يكسان است.درجه حرارت دهانه خروجي كه به اين ترتيب به نقطه جوش مايع مربوط مي شود در طول تقطير ثابت مي ماند.
هرگاه در مايعي تقطير مي شود ناخالصي غير فراري موجود باشد درجه حرارت دهانه خروجي همان درجه حرارت مايع خالص است زيرا ماده اي كه بر روي حباب گرماسنج متراكم مي شود به ناخالصي آلوده نيست.ولي درجه حرارت ظرف به علت كاهش فشا بخار محلول بالا مي ررود. در جريان تقطير درجه حرارت ظرف نيز افزايش مي يابد.زيرا كه غلظت ناخالصي با تقطير جز فرار به تدريج زياد مي شود و فشار بخار مايع بيشتر پايين مي ايد.با وجود اين درجه حرارت دهانه خروجي مانند مايع خالص ثابت مي ماند.رابطه كمي موجود بين فشار بخاروتركيب مخلوط همگن مايع(محلول)به قانون رائول معروف است وبه صورت معادله زيربيان مي شود:
جز مولي Rبه جزيي اطلاق مي شود كه تمام مولكولهاي موجود در آن مولكولهاي Rباشند.براي به دست آوردن اين جز مولي تعداد مولهاي Rدر مخلوط را بر مجموع تعداد مولهاي اجزا سازنده تقسيم مي كنند.معادله در زير آمده است:
بايد دانست كه در بالاي محلول ايده آلي كه محتوي Rاست فشار بخار جزR فقط به جزمولي Rبستگي داردوبه هيچ وجه به فشار بخار اجزاي ديگر مربوط نيست.چنانچه كليه اجزا به غير از Rغير فرار باشند فشار بخار كلي مخلوط برابر با فشار جز Rاست زيرا مي توان فشار بخار تركيبات غير فرار را صفر فرض كرد.در نتيجه محصول تقطير چنين مخلوطي هميشه Rخالص است.ولي اگر دو يا چند جز فرار باشند در اين صورت فشار بخار كل برابر با مجموع فشار بخارهاي جزيي هر يك از اجزاي فرار خواهد شد.(قانون دالتون-در اينجا RوSوTفقط به اجزاي فرار مربوط مي شود):
چنين مخلوط مايعي كه در بالا توضيح داده شد تفاوت زيادي دارد زيرا در اينجا ممكن است محصول تقطير هر يك از اجزاي فراررا در بر داشته باشد.تفكيك دراين حالت احتياج به تقطير جز به جز دارد.چگونگي انجام تقطير جز به جز در ادامه آمده است.
• تقطير تبخير آني (ناگهاني): وقتي محلول چند جزئي مانند نفت خام را حرارت ميدهيم، اجزاي تشكيل دهنده آن بترتيب كه سبكتر هستند، زودتر بخار ميشود. برعكس وقتي بخواهيم اين بخارها را سرد و دوباره تبديل به مايع كنيم، هر كدام كه سبكتر باشد ديرتر مايع ميگردد. با توجه به اين خاصيت ، ميتوانيم نفت خام را به روش ديگري كه به آن "تقطير آني" گويند، تقطير نماييم. در اين روش ، نفت خام را چنان حرارت ميدهيم كه ناگهان همه اجزاي آن تبديل به بخار گردد و سپس آنها را سرد ميكنيم تا مايع شود. در اينجا ، بخارها به ترتيب سنگيني ، مايع ميشوند يعني هرچه سنگينتر باشند، زودتر مايع ميگردند و بدين گونه ، اجزاي نفت خام را با ترتيب مايع شدن از هم جدا ميكنيم.
• تقطير در خلا : با توجه به اينكه نقطه جوش مواد سنگين نفتي نسبتا بالاست و نياز به دما و انرژي بيشتري دارد، و از طرف ديگر ، مقاومت اين مواد در مقابل حرارت بالا كمتر ميباشد و زودتر تجزيه ميگردند، لذا براي جداكردن آنها از خلا نسبي استفاده ميشود. در اين صورت مواد دماي پايينتر از نقطه جوش معمولي خود به جوش ميآيند. در نتيجه ، تقطير در خلا ، دو فايده دارد: اول اين كه به انرژي و دماي كمتر نياز است، دوم اينكه مولكولها تجزيه نميشوند. امروزه در بيشتر موارد در عمل تقطير ، از خلا استفاده ميشود. يعني اين كه: هم تقطير جزء به جزء و هم تقطير آني را در خلا انجام ميدهند.
• تقطير به كمك بخار آب : يكي ديگر از طرق تقطير آن است كه بخار آب را در دستگاه تقطير وارد ميكنند در اين صورت بي آنكه خلاءاي ايجاد گردد، اجزاي نفت خام در درجه حرارت كمتري تبخير ميشوند. اين مورد معمولا در زماني انجام ميشود كه در نقطه جوش آب ، فشار بخار اجزاي جدا شونده بالا باشد تا به همراه بخار آب از مخلوط جدا گردند.
غالبابه كمك تقطير با بخار آب مي توان تركيبات آلي فراري را كه باآب مخلوط نمي شوند يا تقريبا با آن غير قابل اختلاط هستند تفكيك و تخليص كرد.در اين روش مخلوط آب وجسم آلي با هم تقطير مي شوند.عمل تقطير يكمخلوط غير قابل امتزاج در صورتي كه يكي از اجزا آب باشد تقطير با بخار آب ناميده مي شود.
با توجه به اصولي كه در تقطير با بخار آب وجود داردمي توان محاسن ومحدوديت هاي اين روش را به بهترين وجه تشريح كرد.در مخلوطي از مواد فرار و غير قابل اختلاط فشار جزييpiهر جز در يك درجه حرارت معين برابر با فشار بخار piتركيب خالص در همان درجه حرارت استو به جز مولي تركيب در مخلوط بستگي ندارديعني هر يك از اجزاي سازنده مخلوط به طور مستقل از اجزاي ديگر تبخير مي شوند.
اين حالت با مخلوط مايعات قابل اختلاط اختلاف زيادي دارد زيرا كه در اين مايعات فشار جزيي هر جز سازنده به جز مولي آن در محلول مربوط است.(قانون رائول)در مخلوط تركيبات فرار وغير قابل اختلاط بر طبق قانون دالتون فشار كلي Ptمحلول (مخلوط)گازها با مجموع فشارهاي جزيي گازهاي تشكيل دهنده مي شودو به اين ترتيب فشار بخار كلي اين مخلوط از معادله زير به دست مي آيد:
از اين عبارت چنين ر مي آيد كه همواره در هر درجه حرارتي فشار بخار كل مخلوط حتي از فشار بخار فرارترين جز در آن درجه حرارت بيشتر است زيرا كه فشار بخار اجزاي ديگر مخلوط هم دخالت مي كنند.بنابراين بايد درجه جوش مخلوط تركيبهاي غير قابل اختلاط كمتر از جزيي باشد كه كمترين نقطه جوش را دارد.درجه حرارت تقطير با بخار آب نسبتا پايين (100درجه يا كمتراز آن)است و اين تقطير به خصوص در تخليص موادي به كار مي رود كه نسبت به حرارت حساسيت دارندودر حرارت هاي بالا تجزيه مي شوند.هم چنين اين روش براي جدا كردن تركيب از مخلوط از مخلوط واكنشي كه محتوي مقدار زيادي از مواد (قيرمانند)باشد مفيد است.اين مواد غير فرار و بي مصرف در اغلب واكنشهاي آلي تشكيل مي شوند.تركيب درصد محصولي كه در تقطير با بخار آب به دست مي آيد به وزن مولكولي تركيبات مورد تقطير و هم چنين به فشار بخار آنها در درجه حرارت تقطير مخلوط بستگي دارد.مخلوطي از دو جز غير قابل اختلاط AوBرا در نظر بگيريد.چنانچه بخارهاي AوBمانند گازهاي ايده آل عمل مي كنند با استفاده از قانون گازهاي ايه آل مي توان دو عبارت زير را به دست آورد:
از تقسيم معادله اول به دوم چنين به دست مي آيد:
چون فاكتور RTدر صورت و مخرج كسر مساوي است و حجم اشغالي گاز براي هر دو يكسان است(VA=VB)عبارت بالا چنين مي شود:
فرايند تقطير با بخار آب در آزمايشگاه و صنعت به طور وسيعي مورد استفاده قرار مي گيرد .به عنوان مثال براي جداسازي الفاپي نن-آنيلين-نيتروبنزنوبسياري از اسانس هاي طبيعي وروغن هاي معطر به كار مي رود.به طور خلاصه تقطير با بخار آب روشي را فراهم مي كند كه به كمك آن مي توان تركيبات آلي مايع و جامدي را كه فرار هستند ودر آب حل نمي شوند (يا تقريبا در آن نا محلولند)در شرايط نسبتا ملايم از تركيبات غير فرار جدا كرد.مسلما اين روش براي موادي كه در اثر تماس زياد با آب گرم تجزيه مي شوند يا با اب واكنشي مي دهند يا در 100درجه فشار بخارشان 5ميلي متر يا كمتر باشد مناسب نيست.
• تقطير آزئوتروپي : از اين روش تقطير معمولا در مواردي كه نقطه جوش اجزاء مخلوط بهم نزديك باشند استفاده ميشود، جداسازي مخلوط اوليه ، با افزايش يك حلال خاص كه با يكي از اجزاي كليدي ، آزئوتوپ تشكيل ميدهد امكانپذير است. آزئوتروپ محصول تقطير يا ته مانده را از ستون تشكيل ميدهد و بعد حلال و جزء كليدي را از هم جدا ميكند. اغلب ، ماده افزوده شده آزئوتروپي با نقطه جوش پايين تشكيل ميدهد كه به آن شكننده آزئوتروپ ميگويند. آزئوتروپ اغلب شامل اجزاي خوراك است، اما نسبت اجزاي كليدي به ساير اجزاي خوراك خيلي متفاوت بوده و بيشتر است.
مثالي از تقطير آزئوتروپي استفاده از بنزن براي جداسازي كامل اتانول از آب است، كه آزئوتروپي با نقطه جوش پايين با 6/95% وزني الكل را تشكيل ميدهد. مخلوط آب- الكل با 95% وزني الكل به ستون تقطير آزئوتروپي افزوده ميشود و جريان جريان غني از بنزن از قسمت فوقاني وارد ميشود. محصول ته مانده الكل تقريبا خالص است وبخار بالايي يك آزئوتروپي سهگانه است. اين بخار مايع شده، به دو فاز تقسيم ميشود. لايه آلي برگشت داده شده، لايه آلي به ستون بازيافت بنزن فرستاده ميشود. همه بنزن و مقدار الكل در بخار بالايي گرفته شده، به ستون اول روانه ميشوند. جريان انتهايي در ستون سوم تقطير ميشود تا آب خالص و مقداري آزئوتروپ دوگانه از آن بدست آيد.
• تقطير استخراجي : جداسازي اجزاي با نقطه جوش تقريبا يكسان از طريق تقطير ساده مشكل است حتي اگر مخلوط ايده آل باشد و به دليل تشكيل آزئوتروپ ، جداسازي كامل آنها غير ممكن است براي چنين سيستم هايي با افزايش يك جزء سوم به مخلوط كه باعث تغيير فراريت نسبي تركيبات اوليه ميشود، جداسازي ممكن ميشود. جزء افزوده شده بايد مايعي با نقطه جوش بالا باشد، قابليت حل شدن در هر دو جزء كليدي را داشته باشد و از لحاظ شيميايي به يكي از آنها شبيه باشد. جزء كليدي كه به حلال بيشتر شبيه است ضريب فعاليت پايين تري از جزء ديگر محلول دارد، در نتيجه جداسازي بهبود مي يابد اين فرآيند ، تقطير استخراجي نام دارد.
مثالي از تقطير استخراجي، استفاده از فور فورال در جداسازي بوتاديان و بوتن است، فورفورال كه حلالي به شدت قطبي است، فعاليت بوتادي ان را بيش تر از بوتن و بوتان كم ميكند و غلظت بوتادي ان وفورفورال وارد قسمت فوقاني ستون تقطير استخراجي شود، با انجام تقطير بوتادي ان از فورفورال جدا ميشود.
• تقطير جزء به جزء : اجزاي سازنده محلول شامل دو ياچند فرار را كه از قانون رائول پيروي ميكنند، ميتوان با فرايند تقطير جزء به جزء از هم جدا كرد. طبق قانون رائول ، فشار بخار محلول برابر با مجموع اجزاي سازنده آن است و سهم هر جزء برابر با حاصلضرب كسر مولي آن جزء به جزء در فشار بخار آن در حالت خاص است. در تقطير محلولي از B و A ، غلظت A در بخاري كه خارج شده و مايع ميشود، بيش از غلظت آن در مايع باقي مانده است. با ادامه عمل تقطير ، تركيب درصد اجزا در بخار و مايع دائما تغيير ميكند و اين در هر نقطه عموميت دارد. با جمع آوري مايعي كه از سردشدن بخار حاصل ميشود و از تقطير مجدد آن و با تكراري پي در پي اين عمل ، سرانجام ميتوان اجزاي سازنده مخلوط اصلي را به صورتي واقعا خالص بدست آورد.
از نظر سهولت در اينجا فقط محلولهاي ايده آل دو تايي را كه محتوي دو جز فرار RوSباشند در نظر مي گيريم.محلول ايده ال به محلولي اطلاق مي شود كه در آن اثرات بين مولكولهاي متجانس مشابه با اثرات بين مولكولهاي غير متجانس باشد.گرچه فقط محلولهاي ايده ال به طور كامل از قانون رائول پيروي مي كنند ولي بسياري از محلولهاي آلي به محلولهلي ايده آل نزديك هستند.
تقطير جزبه جز محلول هاي غير ايده ال
گرچه بيشتر مخلوط هاي يكنواخت مايع به صورت محلولهاي ايده ال عمل مي كنندولي نمونه هاي بسياري وجود دارد كه نحوه عمل آنها ايده آل نيست.در اين محلولها مولكولهاي غير متجانس در مجاورت يكديگر به طور يكسان عمل نمي كنند انحراف حاصل از قانون رائول به دو روش انجام ميگيرد:
بعضي از محلولها فشار بخار بيشتري از فشار بخار پيش بيني شده ظاهر مي سازندوگفته مي شود كه انحراف مثبت دارند. بعضي ديگر فشار بخار كمتري از فشار پيش بيني شده آشكار مي كنندومي گويند كه انحراف منفي نشان مي دهند.
در انحراف مثبت نيروي جاذبه بين مولكولهاي مختلف دو جز سازنده ضعيف تر از نيروي جاذبه بين مولكولهاي مشابه يك جز است و در نتيجه در حدود تركيب درصد معيني فشار بخار مشترك دو جز بزرگتر از فشار بخار جز خالصي مي شود كه فرارتر است.بنابراين مخلوط هايي كه تركيب درصد آنها در اين حدود باشد درجه جوش كمتري از هر يك از دو جز خالص دارند.مخلوطي كه در اين حدود حداقل درجه جوشش را دارد بايد به صورت جز سوم در نظر گرفته شود.اين مخلوط نقطه جوش ثابتي دارد زيرا تركيب درصد بخاري كه در تعادل با مايع است با تركيب درصد خود مايع برابر است.چنين مخلوطي را آزئوتروپ يا مخلوط آزئوتروپ با جوشش ميني مم مي نامند.از تقطير جز به جز اين مخلوط ها هر دو جز به حالت خالص به دست نمي آيد بلكه جزيي كه تركيب درصد آن از تركيب درصد آزئوتروپ بيشتر باشد توليد مي شود.
در انحراف منفي از قانون رائول نيروي جاذبه بين مولكولهاي مختلف دو جز قويتر از نيروي جاذبه بين مولكولهاي مشابه يك جز است ودر نتيجه تركيب درصد معيني فشار بخار مشترك دو جز كمتر از فشار بخار جز خالص مي شودكه فرارتر است.بنابراين مخلوط هايي كه تركيب درصد آنها در اين حدود باشد حتي نسبت به جز خالصي كه نقطه جوش بيشتري دارد در درجه حرارت بالاتري مي جوشند.در اينجا تركيب درصد به خصوصي وجود دارد كه به آزئو تروپ با جوشش ماكسيمم مربوط مي شود.تقطير جز به جز محلولهايي كه تركيب درصدي غير از تركيب درصد آزئوتروپ دارندباعث خروج جزيي مخلوط مي شودكه تركيب درصد آن از آزئوتروپ بيشتر باشد.
ستونهاي تقطيرجز به جز:
اين ستونها انواع متعددي داردولي در تمام آنها خصلت هاي مشابهي وجود دارد.اين ستونها مسير عمودي را به وجود مي آورند كه بايد بخار در انتقال از ظرف تقطير به مبرد از آن بگذرد.اين مسير به مقدار قابل ملاحظه اي از مسير دستگاه تقطير ساده طويل تر است.هنگام انتقال بخار از ظرف تقطير به بالاي ستون مقداري از بخار متراكم مي شود.چنان چه قسمت پايين اين ستون نسبت به قسمت بالاي آن در درجه حرارت بيشتري نگه داري شود مايع متراكم شده و در حالي كه به پايين ستون مي ريزد دوباره به طور جزيي تبخير مي شود .بخار متراكم نشده همراه بخاري كه از تبخير مجدد مايع متراكم شدهحاصل مي شود در داخل ستون بالاتر مي رود واز يك سري تراكم وتبخير مي گذرد.اين اعمال باعث تقطير مجدد مايع مي شود و به طوريكه در هر يك از مراحل فاز بخاري كه به وجود مي آيد نسبت به جز فرارتر غني تر مي شود.ماده متراكم شده اي كه به پايين ستون مي ريزددر مقايسه با بخاري كه با آن در تماس است در هر يك از مراحل نسبت جزيي كه فراريت كمتري دارد غني تر مي شود.
در شرايط ايده ال بين فازهاي مايع و بخار در سراسر ستون تعادل برقرار مي شود و فاز بخار بالايي تقريبا به طور كامل از جز فرارتر تشكيل مي شود و فاز مايع پاييني نسبت به جزيي كه فراريت كمتري دارد غني تر مي شود.
مهم ترين شرايطي كه براي ايجاد اين حالت لازم است عبارتند از :
1-تماس كامل و مداوم بين فازهاي بخار و مايع در ستون 2-حفظ افت مناسبي از درجه حرارت در طول ستون 3-طول كافي ستون 4-اختلاف كافي در نقاط جوش اجزاي مخلوط مايع.
چنان چه دو شرط اول كاملا مراعات شود مي توان با يك ستون طويل تركيباتي كه اختلاف كمي در نقطه ي جوش دارند به طور رضايت بخش از هم جدا كرد .زيرا طول ستون مورد لزوم و اختلاف نقاط جوش اجزا با هم نسبت عكس دارند.معمول ترين راه ايجاد تماس لازم در بين فازهاي مايع آن است كه ستون با مقدارري ماده بي اثر مانند شيشه يا سراميك يا تكه هاي فلزي به اشكال مختلف كه سطح تماس وسيعي را فراهم مي كندپر شود. يكي از راه هاي بسيار موثر ايجاد اين تماس بين مايع و بخار آن است كه نوار چرخاني از فلز يا تفلون كه با سرعت زياذي در داخل ستون بچرخد به كار رود.
اين عمل نسبت به ستون هاي پر شده اي كه قدرت مشابهي دارند اين مزيت را دارد كه ماده كمي را در داخل ستون نگاه مي دارد(منظور از اين نگه داري مقدار مايع و بخاري است كه براي حفظ شرايط تعادل در داخل ستون لازم است.)
تقطير تبخير ناگهاني
در اين نوع تقطير ، مخلوطي از مواد نفتي كه قبلا در مبدلهاي حرارتي و يا كوره گرم شدهاند، بطور مداوم به ظرف تقطير وارد ميشوند و تحت شرايط ثابت ، مقداري از آنها به صورت ناگهاني تبخير ميشوند. بخارات حاصله بعد از ميعان و مايع باقيمانده در پايين برج بعد از سرد شدن به صورت محصولات تقطير جمع آوري ميشوند. در اين نوع تقطير ، خلوص محصولات چندان زياد نيست.
تقطير با مايع برگشتي (تقطير همراه با تصفيه(
در اين روش تقطير ، قسمتي از بخارات حاصله در بالاي برج ، بعد از ميعان به صورت محصول خارج شده و قسمت زيادي به داخل برج برگردانده ميشود. اين مايع به مايع برگشتي موسوم است. مايع برگشتي با بخارات در حال صعود در تماس قرار داده ميشود تا انتقال ماده و انتقال حرارت ، صورت گيرد. از آنجا كه مايعات در داخل برج در نقطه جوش خود هستند، لذا در هر تماس مقداري از بخار ، تبديل به مايع و قسمتي از مايع نيز تبديل به بخار ميشود.
نتيجه نهايي مجوعه اين تماسها ، بخاري اشباع از هيدروكربنهاي با نقطه جوش كم و مايعي اشباع از مواد نفتي با نقطه جوش زياد ميباشد.در تقطير با مايع برگشتي با استفاده از تماس بخار و مايع ، ميتوان محصولات مورد نياز را با هر درجه خلوص توليد كرد، مشروط بر اينكه به مقدار كافي مايع برگشتي و سيني در برج موجود باشد. بوسيله مايع برگشتي يا تعداد سينيهاي داخل برج ميتوانيم درجه خلوص را تغيير دهيم. لازم به توضيح است كه ازدياد مقدار مايع برگشتي باعث افزايش ميزان سوخت خواهد شد. چون تمام مايع برگشتي بايد دوباره به صورت بخار تبديل شود.
امروزه به علت گراني سوخت ، سعي ميشود براي بدست آوردن خلوص بيشتر محصولات ، به جاي ازدياد مايع برگشتي از سينيهاي بيشتري در برجهاي تقطير استفاده شود. زياد شدن مايع برگشتي موجب زياد شدن انرژي ميشود. براي همين ، تعداد سينيها را افزايش ميدهند. در ابتدا مايع برگشتي را 100درصد انتخاب كرده و بعد مرتبا اين درصد را كم ميكنند و به صورت محصول خارج ميكنند تا به اين ترتيب دستگاه تنظيم شود.
انواع مايع برگشتي
• مايع برگشتي سرد: اين نوع مايع برگشتي با درجه حرارتي كمتر از دماي بالاي برج تقطير برگردانده ميشود. مقدار گرماي گرفته شده ، برابر با مجموع گرماي نهان و گرماي مخصوص مورد نياز براي رساندن دماي مايع به دماي بالاي برج است.
• مايع برگشتي گرم: مايع برگشتي گرم با درجه حرارتي برابر با دماي بخارات خروجي برج مورد استفاده قرار ميگيرد.
• مايع برگشتي داخلي: مجموع تمام مايعهاي برگشتي داخل برج را كه از سينيهاي بالا تا پايين در حركت است، مايع برگشتي داخلي گويند. مايع برگشتي داخلي و گرم فقط قادر به جذب گرماي نهان ميباشد. چون اصولا طبق تعريف اختلاف دمايي بين بخارات و مايعات در حال تماس وجود ندارد.
• مايع برگشت دوراني: اين نوع مايع برگشتي ، تبخير نميشود. بلكه فقط گرماي مخصوص معادل با اختلاف دماي حاصل از دوران خود را از برج خارج ميكند. اين مايع برگشتي با دماي زياد از برج خارج شده و بعد از سرد شدن با درجه حرارتي كمتر به برج برميگردد. معمولا اين نوع مايع برگشتي درقسمتهاي مياني يا دروني برج بكار گرفته ميشود و مايع برگشتي جانبي هم خوانده ميشود. اثر عمده اين روش ، تقليل حجم بخارات موجود در برج است.
نسبت مايع برگشتي
نسبت حجم مايع برگشتي به داخلي و محصول بالايي برج را نسبت مايع برگشتي گويند. از آنجا كه محاسبه مايع برگشتي داخلي نياز به محاسبات دقيق دارد، لذا در پالايشگاهها ، عملا نسبت مايع برگشتي بالاي برج به محصول بالايي را به عنوان نسبت مايع برگشتي بكار ميبرند.
تقطير نوبتي
اين نوع تقطيرها در قديم بسيار متداول بوده، ولي امروزه بعلت نياز نيروي انساني و ضرورت ظرفيت زياد ، اين روش كمتر مورد توجه قرار ميگيرد. امروزه تقطير نوبتي ، صرفا در صنايع دارويي و رنگ و مواد آرايشي و موارد مشابه بكار برده ميشود و در صنايع پالايش نفت در موارد محدودي مورد استفاده قرار ميگيرد. بنابراين در موارد زير ، تقطير نوبتي از نظر اقتصادي قابل توجه ميباشد.
• تقطير در مقياس كم
• ضرورت تغييرات زياد در شرايط خوراك و محصولات مورد نياز
• استفاده نامنظم از دستگاه
• تفكيك چند محصولي
• عمليات توليد متوالي با فرآيندهاي مختلف
تقطير مداوم
امروزه بعلت اقتصادي بودن مداوم در تمام عمليات پالايش نفت از اين روش استفاده ميشود. در تقطير مداوم براي يك نوع خوراك مشخص و برشهاي تعيين شده شرايط عملياتي ثابت بكار گرفته ميشود. بعلت ثابت بودن شرايط عملياتي در مقايسه با تقطير نوبتي به مراقبت و نيروي انساني كمتري احتياج است. با استفاده از تقطير مداوم در پالايشگاهها مواد زير توليد ميشود:
گاز اتان و متان بعنوان سوخت پالايشگاه ، گاز پروپان و بوتان بعنوان گاز مايع و خوراك واحدهاي پتروشيمي ، بنزين موتور و نفتهاي سنگين بعنوان خوراك واحدهاي تبديل كاتاليستي براي تهيه بنزين با درجه آروماتيسيته بالاتر ، حلالها ، نفت سفيد ، سوخت جت سبك و سنگين ، نفت گاز ، خوراك واحدهاي هيدروكراكينگ و واحدهاي روغن سازي ، نفت كوره و انواع آسفالتها.
تقطير ساده:
شكل دستگاه تقطير ساده:
1- شعله 2- بالن ته گرد 3- سه راهي تقطير 4- دماسنج 5- سرد كننده 6- ورودي آب 7- خروجي آب 8- بالن 9- خروج هوا وبخار 10- رابط خلاء
بخش عملي
الف) تقطير ساده تتراكلريدكربن
20 ميلي ليتر تتراكلريد كربن را در بالن تقطير 50 ميلي ليتري بريزيد (احتياط: هرگز از بالني كه بيش از نصف آن از ماده پر شده است استفاده نكنيد) دستگاه تقطير ساده را مطابق شكل سوار كنيد و توجه نمائيد كه حباب دماسنج يا مخزن جيوه اي درست زير بازوي جانبي بالن تقطير (محل خروج بخار از بالن) باشد. قطعه كوچكي از سنگ جوش اضافه كنيد تا امكان تاخير در جوش كه سبب ميشود مايع ناگهاني بالا آيد و يا به طور غير منتظره بداخل مبرد پرت شود، از بين برود.
بالن را با شعله كم حرارت دهيد و طوري شعله را تنظيم كنيد كه سرعت ريختن مايع حاصل از سرد شدن كه از مبرد به داخل ظرف جمع آوري مي ريزد حدود يك قطره در ثانيه باشد. نموداري از تغييرات درجه حرارت نسبت به حجم مايع جمع آوري شده رسم نمائيد و درجه حرارتي كه مايع بيشتري تقطير ميشود به عنوان نقطه جوش ياداشت نمائيد. تقطير را در حالي كه 3-2 ميلي ليتر مايع در بالن تقطير مانده است قطع كنيد.
نقطه جوشي كه به دست آورده ايد با نقطه جوش كربن تترا كلريد كه در كتاب يا مقالات ذكر شده است مقايسه نمائيد.
ب) تقطير ساده متانول و آب
در يك بالن 100 ميلي ليتري مخلوطي از 25 ميلي ليتر متانول و 25 ميلي ليتر آب بريزيد. دو عدد سنگ جوش كوچك در بالن بيندازيد و به آرامي بالن را حرارت دهيد. درجه حرارتي كه اولين قطره مايع از نوك ترمومتر به داخل بالن ميچكد (ميعان) يادداشت كنيد و به عنوان شروع تقطير در نظر بگيريد. در همين لحظه بخارات داخل لوله جانبي شده و مايع ميشود و سرازير شده از دهانه خروجي مبرد وارد ظرف جمع آوري ميشود. در ابتداي شروع تقطير حرارت را به گونه اي تنظيم كنيد كه سرعت تقطير يك قطره در ثانيه باشد. دماي ترمومتر را بر حسب حجم تقطير شده يادداشت كنيد و منحني آنرا رسم كنيد.
در فشار 760 mmHg متانول در 7/64 درجه سانتيگراد و آب در oC 100 مي جوشد. توجه داشته باشيد كه در فشار آزمايشگاه در دماي پايين تري تقطير متانول شروع خواهد شد. هنگامي كه 3-2 ميلي ليتر مايع در ته بالن باقي مانده است تقطيررا متوقف كنيد.
تقطير جزء به جزء:
براي جداكردن موادي كه نقطه جوش آنها خيلي به هم نزديك باشد از تقطير جزء به جزء استفاده ميكنند. اختلاف اين روش با تقطير ساده آن است كه در اين حالت از يك ستون تقطير جزء به جزء استفاده ميشود.
ستونهاي تقطير جزء به جزء انواع متعددي دارند ولي در تمام آنها چند خصلت كلي مشاهده ميشود. اين ستونها مسير عمودي را به وجود مي آورند كه بايد بخار در انتقال از ظرف تقطير به مبرد از آن بگذرد، اين مسير به مقدار قابل ملاحظه اي از مسير دستگاه تقطير ساده طويلتر است. هنگام انتقال بخار از ظرف تقطير به بالاي ستون مقداري از بخار متراكم ميشود. مايع متراكم شده، در حالي كه به پايين ستون مي ريزد دوباره در تماس با بخاري كه از پايين به بالا در جريان است به طور جزئي تبخير ميشود و به سمت بالا ميرود و طي اين ميعان و تبخير شدنهاي متوالي بخار از جزء فرار تر غني تر ميشود، يعني هرچه به سمت بالاي ستون پيش ميرويم غلظت جزء فرار تر بيشتر و هر چه به سمت پايين مي آييم غلظت جزء غير فرار بيشتر ميشود.
از نقطه نظر تئوري، جدا كردن دو تركيب فرار به طور كامل، بوسيله تقطير حتي زمانيكه اختلاف در نقطه جوش آنها زياد باشد امكان پذير نيست زيرا هميشه جزء داراي نقطه جوش پايين تر فشار بخارش را بر روي نقطه جوش جزء ديگر اعمال نموده و پاره اي از مولكولهاي با نقطه جوش بالاتر نيز تقطير ميگردند. اما بهرحال در امور تجربي، بوسيله تقطير جزء به جزء ميتوان مخلوط اينگونه مايعات را در حد مطلوبي جدا نمود.
تقطير جزء به جزء مخلوطهاي دو جزئي و چند جزئي
هدف از تقطير ، جداسازي خوراك به بخارهايي از محصولات تقريبا خالص است در تقطير سيستم هاي دو جزئي ، درجه خلوص با كسر مولي جزء سبك در محصول تقطير XO و در محصول ته مانده XB بيان ميشود. در سيستم هاي دو جزئي از يك مرحله به مرحله ديگر ، به جزء در نقطه آزئوتروپ ، دما و منحني تعادل تغيير ميكنند و يك جزء در تمام ستون فرارتر است. اما در سيستم هاي چند جزئي يك جزء ممكن است در يك قسمت ستون فرارتر و در قسمت ديگر فراريت كمتري داشته باشد، كه ماهيت پيچيده غلظت اجزا را نشان ميدهد. تعادل فازي سيستم هاي چند جزئي نسبت به دو جزئي بسيار پيچيده است، به دليل اينكه تعداد اجزاء زياد است وتعادل به دما بستگي دارد و دما از يك مرحله به مرحله ديگر تغيير ميكند.
شكل دستگاه تقطير جزء به جزء:
1- سنگ جوش 2- مخلوط دو يا چند ماده 3- گرم كننده 4- ظرف تقطير (بالن) 5- ستون تقطير 6- دماسنج 7- خروجي آب 8- ورودي آب 9- سرد كننده 10- رابط خميده ساده 11- ظرف گيرنده (استوانه مدرج) 12- محصول تقطير
مخلوط دو ماده با هم در برخي مواد توليد آزئوتروپ ميكند، يعني مخلوط با درصد معيني تا آخرين قطره تقطير ميشود. در اينگونه موارد نميتوان مخلوط را بوسيله تقطير جزء به جزء از يكديگر جدا كرد. براي از بين بردن اين حالت يا ماده ديگري به مخلوط اضافه ميكنند تا آزئوتروپ ديگري كه مطلوب باشد بدست آيد و يا فشار را تغيير ميدهند. مثلا الكل 95 درصد تشكيل آزئوتروپ ميدهد كه براي از بين بردن نقطه آزئوتروپ، بنزن به آن اضافه ميكنند كه در نتيجه نقطه آزئوتروپ ديگري با درصد آب بيشتر ايجاد ميشود كه بدين ترتيب آب خارج شده، الكل و بنزن باقي ميماند كه بوسيله تقطير جزء به جزء به راحتي جدا ميشود
بخش عملي
الف)تقطير جزء به جزء متانول و آب
در يك بالن ته گرد 100 ميلي ليتري مقدار 30 ميلي ليتر متانول و 30 ميلي ليتر آب بريزيد و براي اطمينان از جوشش آرام (جلوگيري از غليان محلول)، چند عدد سنگ جوش اضافه كنيد دستگاه تقطير جزء به جزء را مطابق شكل سوار كنيد. از ابتداي شروع تقطير حرارت را به گونه اي تنظيم كنيد كه سرعت تقطير 10 الي 20 قطره در دقيقه باشد. درجه حرارتي كه اولين قطره مايع از نوك دماسنج ميچكد را يادداشت كنيد. اگر ستون مايع طغيان ميكند سرعت تقطير را كم كنيد. محصول تقطير (مقطره) را در سه ظرف جدا در محدوده دمايي زير جمع آوري نماييد.
تا دماي 68 درجه مقطره را در ظرف (الف) ذخيره كنيد.
از 68 درجه تا 90 درجه مقطره را در ظرف (ب) جمع آوري نماييد.
از 90 درجه به بعد، آنرا در ظرف (ج) ذخيره كنيد.
تقطير را ادامه دهيد تا 3-2 ميلي ليتر مايع در ظرف تقطير باقي بماند و سپس شعله را خاموش كنيد.
حجم مايعات جمع آوري شده در هر ظرف را اندازه گيري كرده و ياد داشت كنيد. حجم مايع باقي مانده در ظرف تقطير را نيز اندازه گيري نموده و يادداشت كنيد.
ب) تقطير جزء به جزء بنزن و تولوئن
در يك ظرف ته گرد 100 ميلي ليتري 30 ميلي ليتر بنزن و 30 ميلي ليتر تولوئن ريخته و براي اطمينان از جوشش آرام، چند عدد سنگ جوش به آن اضافه كنيد. دستگاه تقطير جزء به جزء را آماده كنيد.
در اين دستگاه محل حباب دماسنج اهميت ويژه اي دارد، به محل آن نسبت به لوله جانبي سر دستگاه تقطير توجه كنيد (شكل دستگاه تقطير). سه ظرف 50 ميلي ليتري به عنوان ظرف گيرنده با برچسب (الف)، (ب) و (ج) آماده كنيد. در عمل بايد نوك رابط خلأ تا داخل گردن اين ظرف امتداد داشته باشد، بين رابط و ظرف گيرنده يك فضاي عمودي باقي نگذاريد زيرا اين فضا باعث سهولت فرار بخارهاي قابل اشتعال ميشود.
ظرف تقطير را با چراغ گاز حرارت دهيد. چراغ را طوري قرار دهيد كه نوك شعله با توري سيمي تماس پيدا كند يا درست زير آن باشد، و شعله را از جريان باد محفوظ نگه داريد به نحوي كه بتوانيد حرارت را تا حد ممكن به دقت تنظيم كنيد. به مجردي كه محلول شروع به جوشيدن كرد و بخارهاي رفلاكس شده به گرما سنج رسيد، شعله را طوري ميزان كنيد كه تقطير فقط با سرعتي در حدود يك قطره مايع مقطر در هر يك يا دو ثانيه به طور يكنواخت ادامه يابد. اولين مايع مقطر را در ظرف گيرنده (الف) جمع آوري كنيد. وقتي كه درجه حرارت دهانه خروجي به 80 درجه رسيد، ظرف گيرنده (الف) را با ظرف گيرنده (ب) و در 105 درجه آن را با ظرف گيرنده (ج) عوض كنيد. تقطير را ادامه دهيد تا حدود 2 ميلي ليتر مايع در ظرف تقطير باقي بماند و بعد شعله را خاموش كنيد. حجم اجزاء تقطير شده در ظرف گيرنده (الف)، (ب) و (ج) را به كمك استوانه مدرج اندازه بگيريد و ياداشت كنيد. اجازه دهيد تا مايع موجود در ستون تقطير به داخل ظرف تقطير برگردد، حجم باقي مانده را اندازه گرفته و يادداشت كنيد.
تقطير با بخار آب:
غالبا به كمك تقطير با بخار آب ميتوان تركيبات آلي فراري را كه با آب مخلوط نميشوند يا تقريبا با آن غير قابل اختلاط هستند تفكيك و تخليص كرد. در اين روش مخلوط آب و جسم آلي با هم تقطير ميشوند. كه به دو صورت امكان پذير است:
1) روش مستقيم: كه مخلوط آب و ماده آلي با همديگر حرارت داده ميشوند (تقطير بوسيله آب).
2) روش غير مستقيم: كه بخار آب را در ظرف ديگري ايجاد كرده و از داخل ماده آلي عبور ميدهند.
در تقطير با بخار آب طبق قانون دالتون فشار بخارهاي حاصله در درجه حرارت معين، برابر با مجموع فشارهاي جزئي همان بخارها است:
PT = P1 + P2 + P3 + …
از اين عبارت چنين بر مي آيد كه همواره در هر درجه حرارتي فشار بخار كل مخلوط حتي از فشار بخار فرار ترين جزء در آن درجه حرارت بيشتر است، زيرا كه فشار بخار اجزاي ديگر مخلوط هم دخالت ميكنند. بنابر اين بايد درجه جوش مخلوط تركيبهاي غير قابل اختلاط كمتر از جزئي باشد كه كمترين نقطه جوش را دارد.
آب (با نقطه جوش 100 درجه) و بروموبنزن (با نقطه جوش 156 درجه) در يكديگر نامحلولند. اين مخلوط در حدود 95 درجه سانتيگراد ميجوشد. در اين درجه، فشار بخار كل مخلوط برابر با فشار آتمسفر است. همانگونه كه طبق نظريه دالتون پيش بيني ميشد اين درجه كمتر از نقطه جوش هر يك از اين دو ماده به صورت خالص است.
مزيت استفاده از تقطير با بخار آب در اين است كه در جه حرارت در اين تقطير نسبتا پايين است (كمتر از 100 درجه) و اين روش براي خالص سازي موادي به كار ميرود كه نسبت به حرارت حساسند و در حرارتهاي بالا تجزيه ميشوند. همچنين اين روش براي جدا كردن تركيب، از مخلوط واكنشي كه محتوي مقدار زيادي از مواد قير مانند باشد مفيد است.
برج تقطير
برجهاي تقطير با سيني كلاهكدار ، تعداد سينيها در مسير برج به نوع انتقال ماده و شدت تفكيك بستگي دارد. قطر برج و فاصله ميان سينيها به مقدار مايع و گاز كه در واحد زمان از يك سيني ميگذرد، وابسته است. هر يك از سينيهاي برج ، يك مرحله تفكيك است. زيرا روي اين سينيها ، فاز گاز و مايع در كنار هم قرار ميگيرند و كار انتقال ماده از فاز گازي به فاز مايع يا برعكس در هر يك از سينيها انجام ميشود. براي اينكه بازدهي انتقال ماده در هر سيني به بيشترين حد برسد، بايد زمان تماس ميان دو فاز و سطح مشترك آنها به بيشترين حد ممكن برسد.
بخشهاي مختلف برج تقطير با سيني كلاهكدار
• بدنه و سينيها: جنس بدنه معمولا از فولاد ريخته است. جنس سينيها معمولا از چدن است. فاصله سينيها را معمولا با توجه به شرايط طراحي ، درجه خلوص و بازدهي كار جداسازي بر ميگزينند. در بيشتر پالايشگاههاي نفت ، براي برجهاي تقطير به قطر 4ft فاصله ميان 50 - 18 سانتيمتر قرار ميدهند. با بيشتر شدن قطر برج ، فاصله بيشتري نيز براي سينيها در نظر گرفته ميشود.
• سرپوشها يا كلاهكها: جنس كلاهكها از چدن ميباشد. نوع كلاهكها با توجه به نوع تقطير انتخاب ميشود و تعدادشان در هر سيني به بيشترين حد سرعت مجاز عبور گاز از سيني بستگي دارد.
• موانع يا سدها: براي كنترل بلندي سطح مايع روي سيني ، به هر سيني سدي به نام "ويير" (Wier) قرار ميدهند تا از پايين رفتن سطح مايع از حد معني جلوگيري كند. بلندي سطح مايع در روي سيني بايد چنان باشد كه گازهاي بيرون آمده از شكافهاي سرپوشها بتوانند از درون آن گذشته و زمان گذشتن هر حباب به بيشترين حد ممكن برسد. بر اثر افزايش زمان گذشتن حباب از مايع ، زمان تماس گاز و مايع زياد شده ، بازدهي سينيها بالا ميرود.
برجهاي تقطير با سينيهاي مشبك
در برجهاي با سيني مشبك ، اندازه مجراها يا شبكهها بايد چنان برگزيده شوند كه فشار گاز بتواند گاز را از فاز مايع با سرعتي مناسب عبور دهد. عامل مهمي كه در بازدهي اين سينيها موثر است، شيوه كارگذاري آنها در برج است. اگر اين سينيها كاملا افقي قرار نداشته باشند، بلندي مايع در سطح سيني يكنواخت نبوده و گذر گاز از همه مجراها يكسان نخواهد بود.
خورندگي فلز سينيها هم در اين نوع سينيها اهميت بسيار دارد. زيرا بر اثر خورندگي ، قطر سوراخها زياد ميشود كه در نتيجه مقدار زيادي بخار با سرعت كم از درون آن مجاري خورده شده گذر خواهد كرد. و ميدانيم كه اگر سرعت گذشتن گاز از حد معيني كمتر گردد، مايع از مجرا به سوي پايين حركت كرده بازدهي كار تفكيك كاهش خواهد يافت.
برجهاي تقطير با سينيهاي دريچهاي
اين نوع سينيها مانند سينيهاي مشبك هستند. با اين اختلاف كه دريچهاي متحرك روي هر مجرا قرار گرفته است. در صنعت نفت ، دو نوع از اين سينيها بكار ميروند:
1. انعطاف پذير: همانطور كه از نام آن برميآيد، دريچهها ميتوانند بين دو حالت خيلي باز يا خيلي بسته حركت كنند.
2. صفحات اضافي: در اين نوع سينيها ، دو دريچه يكي سبك كه در كف سيني قرار ميگيرد و ديگري سنگين كه بر روي سه پايهاي قرار گرفته ، تعبيه شده است. هنگامي كه بخار كم باشد، تنها سرپوش سبك به حركت در ميآيد. اگر مقدار بخار از حد معيني بيشتر باشد، هر دو دريچه حركت ميكنند.
مقايسه انواع گوناگون سينيها
در صنعت نفت ، انواع گوناگون سينيها در برجهاي تقطير ، تفكيك و جذب بكار برده ميشوند. ويژگيهايي كه در گزينش نوع سيني براي كار معيني مورد توجه قرار ميگيرد، عبارت است از: بازدهي تماس بخار و مايع ، ظرفيت سيني ، افت بخار در هنگام گذشتن از سيني ، زمان ماندن مايع بر روي سيني ، مشخصات مايع و ... . چون در صنعت بيشتر سينيهاي كلاهكدار بكار برده ميشوند، براي مقايسه مشخصات سينيهاي ديگر ، آنها را نسبت به سينيهاي كلاهكدار ارزيابي ميكنند.
برجهاي انباشته
در برجهاي انباشته ، بجاي سينيها از تكهها يا حلقههاي انباشتي استفاده ميشود. در برجهاي انباشته حلقهها يا تكههاي انباشتي بايد به گونهاي برگزيده و در برج ريخته شوند كه هدفهاي زير عملي گردد.
1. ايجاد بيشترين سطح تماس ميان مايع و بخار
2. ايجاد فضا مناسب براي گذشتن سيال از بستر انباشته
جنس مواد انباشتي
اين مواد بايد چنان باشند كه با سيال درون برج ، ميل تركيبي نداشته باشند.
استحكام مواد انباشتي
جنس مواد انباشتي بايد به اندازه كافي محكم باشد تا بر اثر استفاده شكسته نشده و تغيير شكل ندهد.
شيوه قرار دادن مواد انباشتي
مواد انباشتي به دو صورت منظم و نامنظم درون برج قرار ميگيرند.
1. پر كردن منظم: از مزاياي اين نوع پر كردن، كمتر بودن افت فشار است كه در نتيجه ميشود حجم بيشتر مايع را از آن گذراند.
2. پر كردن نامنظم: از مزاياي اين نوع پر كردن ، ميتوان به كم هزينه بودن آن اشاره كرد. ولي افت فشار بخار در گذر از برج زياد خواهد بود.
مقايسه برجهاي انباشته با برجهاي سينيدار
در برجهاي انباشته ، معمولا افت فشار نسبت به برجهاي سينيدار كمتر است. ولي اگر در مايع ورودي برج ، ذرات معلق باشد، برجهاي سينيدار بهتر عمل ميكنند. زيرا در برجهاي انباشته ، مواد معلق تهنشين شده و سبب گرفتگي و برهم خوردن جريان مايع ميگردد. اگر برج بيش از حد متوسط باشد، برج سينيدار بهتر است. زيرا اگر در برجهاي انباشته قطر برج زياد باشد، تقسيم مايع در هنگام حركت از بستر انباشته شده يكنواخت نخواهد بود.
در برجهاي سينيدار ميتوان مقداري از محلول را به شكل فرايندهاي كناري از برج بيرون كشيد، ولي در برجهاي انباشته اين كار، شدني نيست. كارهاي تعميراتي در درون برجهاي سينيدار ، آسانتر انجام ميگيرد. تميز كردن برجهاي انباشته ، از آنجا كه بايد پيش از هرچيز آنها را خالي كرده و بعد آنها را تميز نمايم، بسيار پرهزينه خواهد بود.
نكات مهم در انجام عمل تقطير:
1-از دستگاه تقطيري كه رابط هاي آن شل باشند ممكن است بخارهاي قابل اشتعالي كه باچراغ بونزن مجاور مشتعل شود (نشت كند). دستگاهي كه گيره هاي آن سفت بسته شده باشند ممكن است ضمن كار آزمايشگاهي در اثر فشار به نقطه ي شكست خود برسد و علاوه بر خطرات فيزيكي كه شيشه شكسته دارد باعث پخش مواد قابل اشتعال يا سوزان شود.
2-در بستن گيره بايد دهانه گيره با قطعه شيشه اي كه به آن بسته مي شود به صورت موازي قرار گيرد. اين حالت باعث مي شود كه گيره بدون كج كردن شيشه بسته شود وموجب شكستن شيشه يا شل كردن رابط ديگري نشود.قبل از اطمينان از وضعيت درست قطه ي شيشه اي و همترازي صحيح گيره آن را سفت نكنيد.
3-در تقطير ساده دستگاهي كه به كار مي رود در انتهاي گيره خنك كننده به هوا راه داردو از اين راه تعادل فشار برقرار مي شود.در آزمايشگاه هيچگاه نبايد يك دستگاه بسته را حرارت داد. چنان چهت تعادل فشاربرقرار نشود انبساط مواد در دستگاه فشار را زياد ي كند و اين عمل ممكن است باعث انفجار دستگاه شود.
4-در اين آزمايشات بايد توهجه داشت كه موادي مثل بنزن و تولوئن بايد خشك باشند.چنان چه از خشك بودن آنها اطمينان نداريد براي خشك كدن هر يك مي توانيد 50ميلي ليتر از آن را در دستگاه تقطيرساده اي بريزيد و تقطير كنيد تا مايع مقطر كدورتي را نشان ندهد.تقطير را قطع كنيد و باقي مانده تقطير (نه مايع مقطر)را در آزمايش تقطير جز به جز به كار بريد.اين روش براي خشك كردن حلال هاي مر طوبي مناسب است كه با آب آزئو تروپ با جوشش ميني مم مي دهند.
5-هنگاميكه مايع قابل اشتعالي را در حالت تقطير يا رفلاكس حرارت مي دهيد اطمينان حاصل كنيد كه تمام رابط ها نحكم و عاري از فشار باشند.در موقعي كه مايع بسيار فراري را گرم مي كنيد بهتر است كه يك لوله لاستيكي را به دهانه باز دستگاهي متصل مي كنيد و لوله را از لبه بالاي ميز كار بگذرانيد.و آن را از چرا گاز خود دور كنيد.
6-هرگز نگذاريد كه يك محصول تقطير قابل اشتعال به خصوص اگه نزديك به شعله نفر پهلويي شما باشد آزادانه از خنك كننده به ظرف گيرنده اي كه چند اينچ پايين تر از آن است بچكد.براي هدايت محصول تقطير به ظرف گيرنده از يك مبدل استفاده كنيد.
ضميمه:
حلالهاي قابل اشتعال كه معمولا با آنها زياد سرو كار داريم به ترتيب در زير آورده شده است:
1-اتيل اتر
2-استرها(اتيل استات)
3-الكلها(متانول-اتانول-2-پروپانول)
4-كتون ها(استون و بوتانون)
5-كربن دي سولفيد
6-هيدروكربن ها(پنتان -هگزان-بنزن-تولوئن و...)
ارسال : اميرحسين ستوده بيدختي
استفاده از متن مقاله تنها با ذكر منبع اصلي ؛ فرستنده مقاله و نقل از هوپا مجاز است .
منبع:
1)كتاب شيمي آلي تجربي نوين-جلد اول و جلد دوم-نام نويسندگان:رابرتس-گيلبرت-ردوالد-وينگرو-نام مترجم:هوشنگ پير الهي
2)كتاب شيمي عملي و آلي-مولفين:آقايان جليليان-وارسته مرادي-احمدي گلسفيدي
3)technique of chemistry/A.Weissberger
سايت هاي مرتبط:
1)http://www.daneshnamehroshd.com/
2)http://chemlab.mihanblog.com/
3)http://www.distillationgroup.com/distill.htm
4)http://orgchem.colorado.edu/hndbksupport/dist/dist.html
تشخیص آلکان ها :
مقدمه:
پيوند كربن-كربن داراي ويژگي غيرعادي مخصوص به خود است.اگر چه اتم هاي ديگر نيزمي توانند اين ويژگي را داشته باشند ولي كاربرد پيوند كربن-كربن بسيار وسيع است .به دليل اين خاصيت منحصربه فرد بيشتر از سه ميليون تركيبات مختلف حاوي كربن به نام تركيبات آلي در كتب شيمي گزارش شده اند.در نتيجه جمع آوري دانشي كامل از خواص همه اين تركيبات عملا بسيار سخت است.پيچيدگي تركيبات آلي را مي توان تا حدودي از طريق جمع آوري اطلاعات به دست آمده از گروه هاي طبيعي اين تركيبات با خواص شيميايي مشابه تقليل داد.
اين گروه بندي ها توسط اتم يا گروهي از اتم ها كه قسمتي از مولكول آلي را تشكيل مي دهند شناسايي مي شوند.عموما اين اتم يا گره اتم را گروه عامل مي نامند.پس مي توان گروه عاملي را به صورت كامل تري تعريف كرد:
به هر يك از ويژگي هاي ساختاري كه مشخص كننده يك طبقه خاص از تركيبات آلي باشند گروه عاملي مي گويند.
هر گروه عامل نسبت به بقيه مولكول هاي آلي داراي خواص شيميايي جداگانه يافت مي شوند
هيدروكربن ها:
ساده ترين گروه در شيمي آلي هيدروكربن ها بوده كه تركيباتي حاوي ات هاي كربن و هيدروژن مي باشند.با توجه به خواص شيميايي آنها به سه زيرگروه تقسيم مي شوند:هيدروكربن هاي اشباع شده-هيدروكربن هاي اشباع نشده وهيدروكربن هاي آروماتيكي.
هيدروكربن هاي اشباع شده را هم چنين را هم چنين آلكان مي نامنددر آلكان ها همه پيوند هاي كربن-كربن از نوع پيوند ساده بوده كه انرژي پيوندي آن در حدود350كيلوژول مي باشد.انرژي پيوند هاي هيدروژن-كربن در حدود 420كيلوژول است.پس آلكانها از نظر شيميايي تقريبا بي اثر مي باشد.مهم ترين واكنش آنها سوختن است كه آب و دي اكسيدكربن(محصولات سوختن آلكان) توليد مي شوند.
هيدروكربن هاي اشباع نشده داراي 2زير گروه آلكنهاوآلكينها مي باشند.آلكنها داراي يك يا چند پيوند كربن-كربن بوده وآلكينها نيز حاوي يك يا چند پيوند سه گانه كربن-كربن مي باشند .پيوند هاي دو گانه وسه گانه كه پيوند هاي غير اشباع ناميده مي شوند از نظر شيميايي كاملا واكنش پذير مي باشند.
خواص فیزیکی
خواص فیزیکی آلکانها از همان الگویی که برای متان توصیف شد پیروی میکند، و با ساختمان آلکان مطابقت دارد. یک مولکول آلکان کلاً به وسیله پیوندهای کووالانسی ساخته شده است. این پیوندها یا دو اتم مشابه را به یکدیگر متصل میکنند و در نتیجه غیرقطبی میباشند و یا دو اتمی را به هم ربط می دهند که اختلاف الکترونگاتیوی کمی دارند و بنابراین این به مقدار جزئی قطبی هستند. علاوه بر این، این پیوندها به طریقی بسیار متقارن آرایش یافتهاند به طوری که، قطبیت جزئی پیوند نیز حذف میشود. در نتیجه مولکول آلکان یا غیرقطبی است و یا قطبیت خیلی ضعیفی دارد.
نیروهایی که مولکولهای غیر قطبی را به همدیگر مرتبط میکنند (نیروهای واندروالس) نیروهایی ضعیف و با دامنة کوتاه هستند؛ آنها فقط بین قسمتهایی از مولکولهای مختلفی که در تماس نزدیک با یکدیگرند، یعنی بین سطح مولکولها عمل می کنند بنابراین انتظار داریم در یک خانواده، هر چه مولکول بزرگتر باشد – بنابراین، سطح تماس آنها بیشتر است – نیروهای بین مولکولی قویتر باشند.
درجدول بعضی از ثابتهای فیزیکی برای تعدادی از –n آلکانها ذکر شده است. همانطوری که میتوان دید، نقاط جوش و ذوب با افزایش تعداد کربن، زیاد میشود. فرآیند ذوب و جوش نیاز به غلبه بر نیروهای بین مولکولی در جامد و مایع دارد؛ هر چه مولکول بزرگتر شود، نیروهای بین مولکولی زیاد شده و لذا نقطه جوش و ذوب افزایش مییابد.
به جز برای آلکانهای خیلی کوچک، نقطهجوش به ازاء افزایش یک کربن به زنجیر 20 تا 30 درجه زیاد میشود؛ درخواهیم یافت که افزایش 20 تا 30 درجه به ازاء هر کربن، نه تنها در مورد آلکانها بلکه همچنین در مورد کلیه سریهای همردهای که مطالعه میکنیم، صادق است.
افزایش در نقطه ذوب کاملاً منظم نیست، زیرا نیروهای بین مولکولی در یک بلور نه فقط بستگی به اندازه مولکولها دارد بلکه همچنین به چگونگی قرار گرفتن آنها در شبکه بلوری وابسته است.
در نقاط جوش آلکانهایی که ساختمانهای متفاوتی دارند ولی تعداد کربن آنها مساوی است اختلاف نسبتاً کمتری وجود دارد. در صفحات 94 ، 97 نقاط جوش ایزومرهای بوتان، پنتان و هگزان داده شده است. مشاهده میکنیم که در هر مورد، یک ایزومر شاخهای نقطه جوش کمتری از ایزومر راست زنجیر دارد، علاوه بر این، هر چه تعداد شاخهها بیشتر باشد، نقطه جوش پائینتر است به این جهت –n بوتان دارای نقطه جوش و ایزوبوتان میباشد. نقطه جوش –n پنتان ، ایزوپنتان با یک شاخه، و نئوپنتان با دو شاخه میباشد. در تمام خانوادههای ترکیبات آلی، این اثر شاخه بر روی نقطه جوش مشاهده میشود. پائین آمدن نقطه جوش در اثر شاخهای شدن یک پدیده قابل توجیه است: با شاخهای شدن، شکل مولکول به سمت کروی شدن میل میکند، در این صورت اندازه سطح کاهش مییابد، در نتیجه نیروهای بین مولکولی ضعیفتر شده ودر دمای پائینتری مغلوب می شوند. به عنوان مثال، شکل ایزومرهای پنتان را با هم مقایسه کنید.
طبق قاعده «همجنس، همجنس را حل میکند» آلکانها در حلالهای غیرقطبی مانند بنزین، اترو، کلروفرم حل میشوند و در آب و سایر حلالهای خیلی قطبی نامحلولاند. در صورتی که آلکانها را به عنوان حلال در نظر بگیریم، آلکانهای مایع، ترکیبات کم قطبی را در خود حل میکنند و ترکیبات خیلی قطبی را حل نمینمایند.
با افزایش اندازه آلکانها، دانسیته نسبی زیاد میشود، اما در حدود 8/5 ثابت میماند؛ بنابراین تمام آلکانها دانسیتة کمتری از آب دارند تعجبی ندارد که تقریباً تمام ترکیبات آلی دانسیتة کمتری از آب دارند زیرا مانند،آلکانها،به طور عمده از کربن و هیدروژن تشکیل میشوند.
ساختمان پیوند دوگانه کربن- کربن در آلکنها
اتیلن
اتیلن کوچکترین عضو خانوده آلکنها و به فرمول C2H4 میباشد که دو اتم هیدروژن کمتر از آلکان همکربن (اتان) دارد. ما در اینجا به بررسی ساختمان اتیلن میپردازیم تا با ساختار ترکیبات اشباع نشده آشنا شویم. بررسی ساختمان اتیلن به طریق کوانتوم مکانیکی نشان داده است که کربن ، برای اینکه در ساختمان اتیلن شرکت نماید، لازم است که با استفاده از اوربیتالهای 2s و دو اوربیتال 2p خود ، سه اوربیتال هیبریدی یکسان بوجود آورد که این اوربیتالهای هیبریدی ، در یک سطح قرار میگیرند، بنحوی که اتم کربن ، در مرکز یک مثلث قرار گرفته و زوایای بین اوربیتالهای هیبریدی ، 120 درجه تخمین زده شده است.هرگاه ما چهار اتم هیدروژن و دو اتم کربن sp2 را کنار هم مرتب کنیم، شکلی ایجاد میشود که در آن ، هر اتم کربن در سه پیوند σ (سیگما) شرکت دارد. برای رسیدن به کربن به حالت اکتت ، لازم است که سومین اوربیتال 2p اتمهای کربن همپوشانی کرده ، پیوند ایجاد کنند. این پیوند که از همپوشانی اوربیتالهای p کربن ایجاد میشود، از نظر شکل و انرژی ، با پیوند σ متفاوت میباشد و به پیوند π موسوم است که از دو قسمت تشکیل شده است.
یک ابرالکترونی در بالای سطح مولکول و ابر الکترونی دیگر ، در پایین سطح قرار میگیرد. وقتی این ساختمان میتواند انجام شود که تمام اتمهای شرکت کننده در ساختمان اتیلن در یک سطح قرار گیرند. پس مولکول اتیلن لازم است یک مولکول مسطح باشد. مسطح بودن مولکول اتیلن بوسیله روشهای طیف سنجی و پراش الکترونی مورد تایید قرار گرفته است.
پروپن
پروپن به فرمول C3H6 ، CH3-CH=CH2 ، دومین عضو خانواده آلکنها میباشد که سه اتم کربن با 6 اتم هیدروژن به هم متصل شدهاند.بوتن
بوتن به فرمول C4H8 عضو بعدی این خانوده است که برای آن ، چند نوع آرایش میتوان در نظر گرفت که در آنها ، چهار اتم کربن با هشت اتم هیدروژن طوری قرار بگیرند که قانون اکتت رعایت شده باشد. بوتن به ظاهر دارای سه ایزومر میباشد، ولی مطالعات تجربی نشان داده است که برای آلکنی به فرمول C4H8 چهار ساختمان فیزیکی کاملا متفاوت وجود دارد.روش آیوپاک برای نامگذاری آلکنها
در روش آیوپاک ، نامگذاری آلکنها با رعایت نکات زیر انجام میشود:- بلندترین زنجیری را که پیوند دوگانه کربن- کربن در آن قرار گرفته باشد، انتخاب میکنیم.
- زنجیر اصلی را به نحوی شماره گذاری میکنیم که اولین کربن روی پیوند دوگانه ، کوچکترین شماره را به خود بگیرد. (این روش تنها در مورد مشتقات کربن و هیدروژن صادق است. در نامگذاری الکل های اتیلنی و اسیدها و استرهای اتیلنی و برخی مشتقات دیگر ، اولویت با عوامل الکل ، اسید و استر میباشد.)
- شماره کربنهایی را که استخلافها در روی آنها قرار گرفتهاند، مشخص میکنیم.
- اگر قرار باشد ایزومرهای هندسی ماده مشخص گردد، در اول نام ماده از پیشوند cis و trans یا E و Z استفاده میکنیم.
خواص فیزیکی آلکنها
بطور کلی ، خواص فیزیکی آلکنها مشابه آلکانهاست. آلکنها در حلالهای غیرقطبی مانند اتر ، کلروفرم و دیکلرو متان محلول ولی در آب نامحلول میباشند و سبکتر از آب نیز میباشند. نقطه جوش آلکنها با افزایش تعداد کربنها افزایش مییابد. بجز آلکنهای کوچک ، نقطه جوش آلکنها به ازای افزایش یک اتم کربن بین 20 تا 30 درجه سانتیگراد افزایش مییابد. همانند آلکانها ، شاخهدار شدن آلکنها موجب کاهش نقطه جوش میشود.آلکنها اندکی قطبیتر از آلکانها هستند این قطبیت اندک در اثر خصلت الکترون دهی و الکترون گیری گروهها ایجاد میگردد. وقتی روی آلکنها ، گروههای القایی با قدرت بیشتر قرار میگیرد، ممان دو قطبی اندکی افزایش مییابد.
تهیه آلکنها
از طریق هیدروهالوژن زدایی از هالیدهای آلکیل
هیدروهالوژن زدایی ، واکنشی است که طی آن ، از یک مولکول هالید آلکیل یک مولکول هالید هیدروژن (یک اتم هیدروژن از یک کربن و یک اتم هالوژن از کربن مجاور) برداشته میشود. این واکنش بسته به ساختمان و شرایط محلول میتواند از طریق دو مکانیسم متفاوت E2 و E1 انجام بگیرد.تهیه آلکنها از طریق هالوژن ردایی از α- دی بروموآلکان
اگر دو اتم هالوژن در روی یک اتم کربن قرار گرفته باشند، ماده را دیهالوژنه دوقلو geminal مینامند و اگر دو هالوژن در روی دو اتم کربن مجاور قرار گرفته باشند، vicinal خوانده میشود. از واکنش مشتقات α- دی برومو با پودر روی در اسید استیک و طی یک واکنش هالوژن زدایی ، آلکن مربوطه تولید میشود. در این واکنش ، هر دو اتم برم آزاد میشود و آلکن تشکیل میگردد. روی در اسید استیک نقش احیا کننده را بازی میکند. روی اکسید میشود و هالید الکیل احیا میشود.تهیه آلکنها از طریق آبگیری از الکلها
یکی از بهترین روشهای تهیه آلکنها ، آبگیری از الکلهاست. واکنش آبگیری از الکل در حضور کاتالیزورهای اسیدی ، معمولا برگشت پذیر بوده ، سرعت کمتری دارد. لذا جهت جلوگیری از واکنش برگشتی و برای تکمیل واکنش ، آلکن تولید شده را از محیط واکنش خارج میکنند. با توجه به این که نقطه جوش آلکنها ، پایینتر از نقطه جوش الکلهای مربوطه میباشد، لذا این عمل بسهولت انجام میگیرد. در واکنشهای آبگیری از الکلها ، معمولا از اسید سولفوریک یا اسید فسفریک غلیظ استفاده میشود.واکنشهای شیمیایی آلکنها
اگر بخواهیم واکنشهای شیمیایی آلکنها را پیشبینی نماییم، لازم است ابتدا فعالیت پیوند π در آلکنها را مورد مطالعه قرار دهیم و تاثیر پیوند دوگانه روی گروههای آلکیل مجاور و برعکس را خوب بدانیم. با مطالعه واکنشهای اختصاصی پیوند دوگانه ، قادر خواهیم بود تا واکنشهای اختصاصی خیلی از آلکنها و واکنشگرهای دیگر را پیشبینی نماییم.
بطور کلی دو نوع واکنش در روی آلکنها انجام پذیر میباشد. دسته اول آنهایی هستند که در روی پیوند π انجام میگیرند و لذا پیوند π از بین میرود و پیوندهای جدید تشکیل میگردد. واکنشهای دسته دوم ، واکنشهایی هستند که در محلولهای دیگری که ارتباط خاصی با پیوند دوگانه دارند، اتفاق میافتند. مثل گروههای آلکیل و یا عوامل دیگری که به کربنهای sp2 متصل میباشند.
بهترین راه شناسایی آلکنها
تجربه شنان داده است که بهترین راه شناسایی یک آلکن ، خاصیت رنگ زدایی آن در محلول برم در تتراکلرید کربن و در محلول سرد ، رقیق و خنثای پرمنگنات است. انجام هر دو آزمون آسان است. در یکی ، رنگ قرمز از بین میرود و در دیگری رنگ بنفش جای خود را به دیاکسید منگنز قهوهای میدهد.
اشکال و ابهام در شناسایی
پس از انتخاب بهترین آزمونها برای شناسایی آلکنها ، به پرسش دیگری میپردازیم. برم در تتراکلرید کربن را به یک ترکیب ناشناخته آلی اضافه میکنیم و فرض کنید رنگ قرمز از بین میرود. راستی از این پدیده چه نتیجهای میتوان گرفت؟ فقط میتوان گفت که ماده ناشناس ما با برم ترکیب میشود. البته ممکن است یک آلکان باشد.
آگاهی از اینکه نوع معینی از ترکیبها با یک واکنشگر خاص و مشخص واکنش میدهند، خودبهخود کافی نیست. بلکه بایستی بدانیم کدام ترکیبهای دیگر نیز با این واکنشگر واکنش میدهند؟ در این مورد ، ترکیب ناشناس ممکن است یک آلکین هم باشد. همچنین ممکن است هر ترکیب دیگری که به سرعت با برم واکنش جانشینی میدهد، باشد. البته در این صورت گاز برمید هیدروژن متصاعد خواهد شد که سادهترین راه تشخیص آن ، دمیدن به درون لوله آزمایش و مشاهده توده ابری تشکیل شده ، است.
همینطور ، رنگ زدایی پرمنگنات ، آلکن بودن ترکیبی را به اثبات نمیرساند، بلکه فقط وجود نوعی گروه عاملی اکسید شونده با پرمنگنات را نشان میدهد. ترکیب مورد آزمایش ، ممکن است یک آلکن باشد، اما احتمال اینکه آلدئید آلکین یا هر ترکیب دیگری که به سهولت اکسید میشود، نیز وجود دارد. حتی ممکن است ترکیبی باشد که حاوی مقداری ناخالصی اکسید شونده است. برای مثال ، آلکنها در چنین شرایطی اکسیده نمیشوند، ولی اغلب ، ناخالصیهایی دارند که اکسید شونده است. برای مثال ، الکلها ، در چنین شرایطی اکسیده نمیشوند، ولی اغلب ، ناخالصیهای دارند که اکسیده میشوند. برای رفع این ابهام ، میتوان از رنگ زدایی دو سه قطره از واکنشگر اطمینان حاصل کرد.
با یک آزمون شناسایی ، به ندرت میتوان نوع ترکیب مجهول را اثبات کرد. یک آزمون فقط میتواند شمار احتمالها را کاهش دهد، به گونهای که با آزمونهای اضافی دیگری ، تصمیم گیری نهایی امکانپذیر شود. در نتیجه ، آزمون برم یا پرمنگنات برای تشخیص آلکن از آلکان ، یا آلکن از آلکیل هالید ، یا آلکن از الکل کافی است.
روشی دیگر برای شناسایی آلکن
روش انحلال پذیری آلکنها در اسید سولفوریک سرد و غلیظ نیز مفید است. آزمونی که شمار زیادی از ترکیبها ، شامل مواد اکسیژندار ( که نمکهای انحلالپذیر اکسونیوم تولید میکنند.) و ترکیباتی که به آسانی سولفوردار میشوند، به ؟آن پاسخ مثبت میدهند. آلکانها یا آلکیل هالیدها در اسید سولفوریک سرد و غلیظ حل نمیشوند. سیکلوپروپان به آسانی در اسید سولفوریک غلیظ حل میشود، اما بوسیله پرمنگنات اکسیده نمیشود.
الکلها و اترها نیز در اسید سولفوریک حل میشوند، اما با استفاده از پاسخ منفی این ترکیبها به آزمون برم در تتراکلرید کربن و آزمون با ید ، میتوان آنها را از آلکنها تشخیص داد، البته به شرطی که بوسیله ناخالصیها گمراه نشویم. الکلهای نوع اول و نوع دوم بوسیله ایندرید کرومیک ، 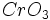 ، در اسید سولفوریک آبی اکسید میشود. طی دو ثانیه محلول نارنجی شفاف به رنگ آبی مایل به سبز در آمده و سپس مات میشود.
، در اسید سولفوریک آبی اکسید میشود. طی دو ثانیه محلول نارنجی شفاف به رنگ آبی مایل به سبز در آمده و سپس مات میشود.
الکلهای نوع سوم ، اترها و آلکنها به این آزمون پاسخ مثبت نمیدهند. آلدئیدها پاسخ مثبت میدهند، اما با روشهای دیگری تشخیص داده میشوند..
توضیحات کامل درباره واکنش های آلکن ها



Determination of alkenes in cracking products
[Alkene bromination used for detailed hydrocarbon
مفاهیم اولیه
آلکیل هالیدها همانطور که از نامشان پیدا است آلکیلهایی هستند که با هالوژن پیوند تشکیل دادهاند. این ترکیبات دارای فرمول عمومی R-X هستند که R یک گروه آلکیل و یا گروه آلکیل استخلاف شده و X اتم هالوژن است. آلکیل هالیدها معمولا از الکل تهیه میشوند و نقطه آغاز سنتز برای بسیاری از مواد هستند. مشخصترین واکنشهای آنها واکنشهایی هستند که روی گروه عاملی آنها ( اتم هالوژن ) انجام میشوند. آلکیل هالیدها در آب نامحلولاند اما در حلالهای آلی مانند بنزن ، اتر ، کلروفرم و... محلول هستند.خواص فیزیکی
آلکیل هالیدها در مقایسه با آلکیل اولیهای که از آن بوجود آمدهاند بخاطر وزن مولکولی بیشتر دمای جوش بالاتری دارند. بعنوان مثال هالو آلکنها در مقایسه با آلکانهایی با تعداد کربن برابر دمای جوش بالایی دارند. در یک گروه آلکیل معین با افزایش وزن اتمی هالوژن دمای جوش افزایش مییابد. فلوئورورها زود جوشترین و یدیدها دیر جوشترین هالیدها هستند.شاخهدار شدن در گروههای آلکیل یا در کربن دارای پیوند هالوژن سبب پایین آمدن دمای جوش نسبت به آلکیل هالیدهای راست زنجیر با همان تعداد کربن میشود. با وجود قطبیت متوسطی که دارند در آب نامحلولند که علت احتمالی آن میتواند ناتوانی در تشکیل پیوندهای هیدروژنی باشد. این ترکیبات حلالهای خوبی برای سایر ترکیبات با قطبیت کم از جمله خودشان هستند و چون نمیتوانند یونهای ساده را بطور قابل ملاحظهای حلال پوشی کنند نمکهای معدنی در آنها نامحلول هستند. آلکیل هالیدهای دارای یدید برمید و پلی کلرها چگالتر از آب هستند.
طبقهبندی آلکیل هالید
آلکیل هالیدها را با توجه به اینکه کربن حامل هالوژن ، به چند گروه آلکیل متصل است طبقهبندی میکنند.- آلکیلهای نوع 1 : کربن حامل هالوژن را با یک گروه آلکیل پیوند دارد.
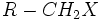
- الکیلهای نوع 2 : کربن حامل هالوژن با دو گروه آلکیل پیوند دارد.
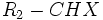
- آلکیلهای نوع 3 : کربن حامل هالوژن با سه گروه آلکیل پیوند تشکیل داده است.
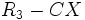
تهیه آلکیل هالیدها
- آلکیلها را معمولا از الکلها که قابل دسترستر هستند تهیه میکنند. برخی از آلکنها در جریان جایگزین شدن گروه –OH با -X میل به نو آرایی دارند، اما با استفاده از فسفر هالیدها میتوان مانع نوآرایی شد. روشهای دیگر تهیه آلکیل هالیدها عبارت است از:
- یک آلکیل یدید غالبا از آلکیل برمید یا آلکیل کلرید مربوطه در اثر واکنش با محلول سدیم یدید در استون تهیه میشود.
واکنشهای آلکیل هالیدها
- جانشین هستهدوستی : آلکیل هالیدها در حضور یک هستهدوست که معمولا یک باز است واکنش انجام میدهند که در اثر این واکنش هستهدوست جایگزین هالوژن میشود.
- واکنش حذفی : آلکیل هالیدها در حضور باز در اثر فرایند هیدرو هالوژنزدایی یک هیدروکربن غیر اشباع ایجاد میکنند.
تهیه واکنشگر گرینیارد
آلکیل هالیدها در حضور اتر خشک با فلز منیزیم واکنش نشان داده و واکنش گرینیارد ( RMgX ) را ایجاد میکنند. این ترکیبات میتوانند در حضور فلز و اسید به آلکیل اولیه احیا شوند.شناسایی آلکیل هالیدها
مهمترین روش شناسایی آلکیل هالیدها این است که به مدت چند دقیقه با محلول الکلی نیترات نقره حرارت داده شوند. با تشکیل رسوبی که در اسید نیتریک رقیق نامحلول است هالوژن شناسایی میشود. ترکیب واکنشپذیری هالیدهای معین با نیترات نقره بصورت RI> RBr> RCL است و در مورد یک هالوژن معین واکنش آلکیل هالیدها بصورت > 2> 1 آلکیل هالید 3 درجه است. 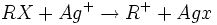
Silver Nitrate Solution (Ethanolic)
Alkyl Halide
![]()
Acyl Halide

Procedure
This reagent is useful for classifying compounds known to contain halogen. Add 1 drop or a couple of crystals of the unknown to 2 mL of the 2% ethanolic silver nitrate solution. If no reaction is observed after 5 min standing at room temperature, heat the solution to boiling and note if a precipitate is formed. If there is a precipitate, note its color. Add 2 drops of 5% nitric acid, and note if the precipitate dissolves. Silver halides are insoluble in dilute nitric acid; silver salts of organic acids are soluble.
Positive Test
alkyl halide - Production of solid silver halide salt is a positive test.
acyl halide - Production of solid silver carboxylate salt is a positive test. This solid should redissolve in dilute nitric acid
Complications
The time and temperature required to form the solid salt can vary widely
Alkyl Halide
![]()
Sulfonyl Chloride
![]()
Acyl Halide

ضریب شکست نور در مایعات مجهول
یکی دیگر از راههای شناسایی و تشخیص ترکیبات آلی استفاده از ثابت فیزیکی ضریب شکست نور در یک مایع مجهول میباشد.
سرعت انتقال نور در محیطهای مختلف متفاوت است. انحراف شعاع نور در هنگام عبور از حد فاصل دو محیط مختلف یکی از نتایج مستقیم و قابل رویت این اختلاف است. انحراف نور به علت تغییر سرعت آن است.
زاویه شکست نور (زاویه انحراف) به دانسیته محیط، نوع مولکولهای موجود، درجه حرارت محیط و طول موج نور بستگی دارد. چنانچه محیطی مانند هوا به عنوان مقیاس انتخاب شود و زوایای شکست با یک طول موج یکنواخت در یک درجه حرارت یکسان اندازه گیری شود، در این صورت زوایای اندازه گیری شده یکی از خواص محیط ثانوی در حد فاصل مربوط است و میتوان از آن به عنوان یک خصلت مشخص جسم سازنده آن محیط استفاده کرد.
مقداری که عملا به صورت ثابت فیزیکی یک مایع گزارش میشود، زاویه شکست آن نیست بلکه ضریب شکستی (n) است که از معادله زیر تعیین میشود:
n=sin i / sin p
در اینجا i زاویه ای است که نور ورودی (در هوا) با خط عمود بر سطح حد فاصل میسازد و p زاویه ای است که نور شکسته شده (در مایع) با این خط به وجود می آورد. نور تکفام مقادیر دقیق تری از نور معمولی میدهد و از این جهت ضرایب شکست را اکثرا نسبت به خط D سدیم (598.3 mμ = λ طول موج) گزارش میکنند. این نور را به صورت پایه و درجه حرارت را به صورت توان نشان میدهند (مانند nD20 = 1.3330).
رفراکتومتر Abbe دستگاهی است که غالبا شیمیدانها از آن استفاده میکنند. در این رفراکتومتر از نور معمولی به عنوان منبع نور استفاده میشود، ولی با یک موازنه ای که در یک سیستم منشوری به عمل می آید، ضریب حاصل نسبت به خط D سدیم به دست می آید.


کربوهیدراتها (هیدراتهای کربن یا مواد قندی) یکی از انواع مولکولهای زیستی هستند که از نظر شیمیایی آنها را پلیهیدروکسیآلدئید یا پلیهیدروکسیکتون میدانند. هیدراتهای کربن از اتمهای کربن، هیدروژن و اکسیژن تشکیل شدهاند. کربوهیدراتهادر بدن بیشتر به عنوان مولکولهای ذخیرهکننده انرژی عمل میکنند، اما کاربردهای ساختاری و نقش در انتقال پیام و... نیز دارند.
|
فهرست مندرجات |
ساختار
کربوهیدراتهای خالص شامل اتمهای کربن، هیدروژن، و اکسیژن هستند با نسبت ملکولی ۱:۲:۱ که فرمول عمومی Cn(H۲O)n را تشکیل میدهند. با این وجود، خیلی از کربوهیدراتهای مهم از این قانون مستثنی هستند (مثل دیوکسیریبوز و گلیسرول که بدین ترتیب آنها را مستقیما نمیتوان کربوهیدرات خواند.با افزایش طول زنجیر، تعداد کربنهای با مراکز فضایی افزایش مییابند و بدین ترتیب تعداد زیادی دیاسترومر امکانپذیر میشوند. قندها ترکیبات پلی هیدروکسی کربونیل اند، از این رو میتوانند هِمی استالهای حلقوی پایداری ایجاد کنند، بدین ترتیب ساختارهای اضافی و تنوع شیمیایی برای این ترکیبات پدید میآید. گاهی وقتها ترکیباتی که شامل عناصر دیگری نیز میشوند را هم کربوهیدرات میخوانند(مثلاً چیتین که شامل نیتروژن نیز است).کربوهیدراتها همچنین به عنوان واحدهای سازنده برخی چربیها و نوکلئیک اسیدها عمل میکنند.
دستهبندی کربوهیدراتها
کربوهیدراتها یا به صورت تک واحدی هستند (تکقندیها یا مونوساکاریدها) و یا بصورت دیمر، تریمر و یا پلیمرهایی از این زیر واحدها هستند که به ترتیب دوقندیها (یا دیساکارید)ها، چندقندیها (یا الیگوساکاریدها) و پلیساکاریدها نامیده میشوند. یک منوساکارید یا قند ساده، یک آلدئید یا کتونی با حداقل دو گروه هیدروکسیل است. بدین ترتیب دو عضو ساده این طبقه از ترکیبات، ۲ و ۳ - دی هیدروکسی پروپانال (گلیسرآلدئید)، ۱ و ۳ - دی هیدروکسی پروپانون (۱ و ۳ - دی هیدروکسی استون) میباشند. قندهای پیچیده از اتصال قندهای ساده همراه با حذف آب بدست میآیند. قندهای آلدئیدی بصورت آلدوزها طبقه بندی میشوند. آنهایی که عامل کتونی دارند، کتوز خوانده میشوند. بر اساس طول زنجیر، قندها، تریوز (۳ کربنی)، تتروز (۴ کربنی)، پنتوز (۵ کربنی)، هگزوز (۶ کربنی) و غیره نامیده میشوند. از اینرو، ۲ و ۳ - دی هیدروکسی پروپانول (گلیسرآلدئید) یک آلدوتریوز است. در حالی که ۱ و ۳ - دی هیدروکسی پروپانون یک کتوتریوز میباشد.
تکقندیها
گلوکز، قند خون یا قند انگور (گلایکیس، در فرهنگ یونانی به معنی شیرین) که به دکستروز موسوم است، یک پنتاهیدروکسی هگزانال بوده، از اینرو در خانواده آلدوزهگزوزها جای دارد. گلوکز بصورت طبیعی در بسیاری از میوهها و گیاهان با غلظتی در گستره ٪۰٫۰۸ تا ۰٫۱٪ در خون انسان وجود دارد.
ایزومر کتوهگزوزی گلوکز، فروکتوز است. فروکتوز شیرینترین قند طبیعی است (برخی از قندهای سنتزی شیرینترند). فروکتوز نیز در بسیاری از میوهها (فروکتوز در فرهنگ لاتین به معنی میوه) و در عسل وجود دارد.
قند طبیعی مهم دیگر آلدوپنتزو ریبوز است. این قند واحد ساختاری ریبونوکلئیک اسیدها میباشد. فرمول ساده یا تجربی برای همه قندها میباشد. این فرمول، هم ارز فرمول هیدرات کربن است. این یکی از دلایلی است که به این دسته از ترکیبات کربوهیدرات گفته میشود.
دوقندیها
دیساکارید از تشکیل دو مونوساکارید از طریق تشکیل یک پل اتری (معمول استال) بدست میآید. آبکافت دیساکاریدها، منوساکاریدها را دوباره بدست میدهد.
لاکتوز یا قند شیر، ساکاروز یا شکر و مالتوز یا قند مالت، نمونههایی از دیساکاریدها هستند.
پلیساکاریدها
تشکیل اتر بین یک منو و یک دیساکارید یک تریساکارید ایجاد میکند و تکرار این فرآیند نهایتا به تولید یک پلیمر طبیعی (پلیساکارید) منجر میشود. چنین کربوهیدراتهای پلیمری، تشکیلدهنده اسکلت اصلی سلولز و نشاسته هستند. مهمترین پلیساکاریدها شامل:
-
نشاسته یا آمیلون
میباشند.
نشاسته کربوهیدرات ذخیرهای در گیاهان (سیب زمینی، ، نان، برنج و...) است که از بهم پیوستن تک قندیها به اشکال مختلف حاصل میشوند و در بدن پس از گوارش مالتوز تبدیل شده و سرانجام به تکقندیهای گلوکز، فروکتوز و گالاکتوز در میآیند. این سه تکقندی جذب خون شده و پس از عبور از کبد به وسیله گردش خون در سرتاسر بدن پخش میگردد.
آمیلوز، پلیمر خطی گلوکز است
گلیکوژن تنها شکل ذخیره انرژی به صورت قند در بدن انسان است. مقدار ذخیره گلیکوژن در انسان ۳۵۰ گرم است. حدود ۱۰۰ یا ۱۰۸ گرم گلیکوژن در کبد است و بقیه در ماهیچههاست. مقدار ذخیره گلیکوژن در بدن انسان به اندازه این است که نیازهای نصف روز انسان را تأمین میکند. بدین صورت که فردی گرسنهاست و غذا نمیخورد، گلیکوژن کبدی، قند خون وی را تأمین میکند و گلیکوژن ماهیچهها، نیازهای عضلانی را تأمین میکند. زمانی که گرسنگی دوم اتفاق میافتد، زمانی است که گلیکوژن کبدی تخلیه شده و گلیکوژن که تحت تأثیر زیمایه (آنزیم) فسفریلاز قرار میگیرد گلیکوژن کبدی است نه گلیکوژن ماهیچه.
سلولز نیز پلیساکاریدی است که در گیاهان تولید میشود. تفاوت ساختمانی آن با نشاسته این است که در سلولز پیوندهای بتا ۱ به ۴ وجود دارد اما در روده پستانداران آنزیمی برای تجزیه آن وجود ندارد. در روده نشخوار کنندگان سلولز توسط آنزیم سلولاز که توسط باکتریهای رودهای آنها تولید میشود تجزیه میشود.
سوختوساز کربوهیدراتها
کربوهیدراتها به گلوکز تبدیل میشوند و گلوکز به دو طریق در بدن دگرگشت یا سوختوساز (متابولیسم) هوازی میشود:
دگرگشت هوازی گلوکز: بدین صورت که ابتدا مولکول گلوکز میشکند و دو مولکول اسید پیرویک ایجاد میکند، اسد پیرویک دکربکسیله میشود و به مشتق استیل تبدیل میشود، مشتق استیل با کوآنزیم A ترکیب میشود و استیل کوآنزیم A را ایجاد میکند. استیل کوآنزیم A وارد چرخه کرپس میشود و طی یک سلسله واکنشهای پیاپی به آب، انرژی و CO۲ تبدیل میشود.
دگرگشت بیهوازی: زمانی که بدن در شرایط اضطراری قرار میگیرد متابولیسم بی هوازی رخ میدهد. مثلاً ورزشکاری که فعالیت سنگین انجام میدهد، قادر به تأمین کل انرژی مورد نیاز خود از طریق هوازی نیست، قسمتی از انرژی خود را از طریق بی هوازی تأمین میکند. یا در شرایطی که فرد در حالت خفگی قرار میگیرد (آب یا دود) بدن از طریق متابولیسم بی هوازی سعی در حفظ حیات میکند. بدین صورت که مولکول گلوکز میشکند، دو مولکول اسید پیروویک ایجاد میکند، هر مولکول اسید پیروویک احیاء میشود و اسید لاکتیک ایجاد میکند. علت اینکه اسید لاکتیک باعث گرفتگی ماهیچه یا خستگی ورزشکاران میشود، متابولیسم بی هوازی است. بنابراین در شرایط بی هوازی از متابولیسم گلوکز دو ATP (آدنوزین تری فسفات) و در شرایط هوازی از متابولیسم گلوکز سی و هشت ATP انرژی حاصل میشود. البته ممکن است تصور کنید هضم دگرگشت بی هوازی باعث تخریب انرژی میشود در صورتیکه اسید لاکتیک جمع شده در ماهیچه با جریان خون به کبد میرود و مجدداً تبدیل به گلیکوژن میشود و دوباره قند میسازد.
ساختار تمام کربوهیدراتها یکسان نیست. کربوهیدراتهای ساده که در چیپس، کلوچه و نان سفید وجود دارند به سادگی هضم میشوند اما کربوهیدراتهای مرکب که در میوهها و سبزیها و نان جو و سایر حبوبات وجود دارند به سرعت هضم نشده و درصد سوخت آنها پایین است. [۱]
کارکرد مواد قندی و نشاسته در بدن
تولید گرما نقش اصلی و عمده این مواد تولید انرژی در بدن است. تنظیم قند خون بدن سالم بعد از جذب قندها به وسیله اعمالی که انجام میدهد، مقدار آن را تا حدودی ثابت نگه میدارد. ذخیره در بدن مقدار اضافی مواد قندی و نشاستهای در کبد و ماهیچهها به میزان معینی ذخیره و بقیه به صورت چربی در بافت چربی ذخیره میگردد تا در صورت لزوم، بدن بتواند به عنوان منبع انرژی از آن استفاده نماید.
فعالیت نوری قندها
به استثنا ۱ و ۳ - دیهیدروکسی- پروپانون، همه قندهایی که تاکنون ذکر شدهاند، حداقل حاوی یک مرکز فضاییاند. سادهترین قند کایرال، ۳ و ۲ - دیهیدروکسی پروپانون (گلیسرآلدئید) با یک کربن نامتقارن است. فرم راستبر آن R است، به صورتی که در طرحهای فیشر مولکول نشان داده میشود، انانتیومر چپبر آن، S میباشد.
گر چه نامگذاری S و R برای نامیدن قندها کاملا رضایت بخش است، اما سیستم نامگذاری قدیمی هنوز بکار گرفته میشود. این سیستم نامگذاری، قبل از تدوین پیکربندی مطلق قندها متداول بوده، همه قندها را به ۲ و ۳ - دیهیدروکسی پروپانال (گلیسرآلدئید) مرتبط میسازد. در این روش بجای استفاده از S و R از پیشوند D برای انانتیومر (+) وL برای انانتیومر (-) گلیسرآلدئید استفاده میشود.
قندها، تشکیلدهنده همیاستالهای درون مولکولی
قندها ترکیبات هیدروکسی کربونیلاند و بایستی قادر به تشکیل درون مولکولی همی استال باشند. در واقع گلوکز و سایر هگزوزها و پنتوزها به صورت مخلوط در حال تعادل با ایزومرهای حلقوی همیاستال خود هستند. در این مخلوط در حال تعادل، ایزومر حلقوی همیاستال برتر است. در اصل هر یک از پنج گروه هیدروکسی میتوانند به گروه کربونیل آلدئید افزوده شوند. اما گرچه حلقههای پنج ضلعی نیز شناخته شده هستند، حلقههای شش ضلعی معمولا محصول برتر میباشند.
[ویرایش] گسستگی اکسایشی قندها
واکنشگری که باعث شکستن پیوند C-C میشود، پریدیک اسید (HIO۴) است. این ترکیب دیالهای مجاور را اکسایش کرده، ترکیبات کربونیل ایجاد میشوند. از آنجا که اغلب قندها چندین دیال مجاور دارند، اکسایش با HIO۴مخلوط پیچیدهای ایجاد میکند. مقدار کافی از اکسنده، زنجیر قند را بطور کامل به ترکیبات یک کربنی تبدیل میکند.
از این روش برای شناسایی ساختار قندها استفاده میشود. مثلا از مجاورت گلوکز با ۵ اکی والان HIO۴، پنج اکی والان فرمی اسید و ۱ اکی والان فرمالدئید بدست میآیند. در اکسایش فروکتوز ایزومری نیز همان مقدار عامل اکسنده مصرف شده، اما محصولات، ۳ اکی والان اسید، ۲ اکی والان آلدئید و یک اکی والان دیاکسید هستند.
انرژیزایی کربوهیدراتها
کربوهیدراتها انرژیزا هستند و انجام اعمال حیاتی را تسهیل مینمایند، از اینرو از بهترین مواد تغذیهای برای ورزشکارانند. مواد قندی و نشاستهای یکی از مهمترین و ارزانترین منابع انرژی در رژیم غذایی انسان بشمار میروند. قسمت مهمی از غذاهای مردم آسیا، آفریقا و بسیاری از نقاط جهان از مواد قندی و نشاستهای تشکیل شدهاست. به علت ارزانی کربوهیدراتها، اکثر مردم از آنها استفاده میکنند و ۴۰ تا ۵۰ درصد غذای روزانه را تشکیل میدهند. هنگامی که کربوهیدراتها وارد بدن میشوند به انرژی تبدیل میگردند و مقدار اضافی آنها در بافتهای چربی ذخیره میشود. در همه نقاط دنیا یک ماده غذایی نشاستهای، غذای اصلی مردم است. در بیش از ۵۰ درصد کشورهای دنیا برنج، گندم، ذرت، سیب زمینی و نان، را به عنوان غذای اصلی استفاده میکنند. مشتقات تک قندیها، سوریبتول است که از احیای گلوکز به دست میآید. ویژگی آن سرعت جذب خیلی کند است. بنابراین به طور کامل جذب نمیشود. سرعت کند جذب سوریبتول در چند زمینه مورد استفاده تغذیهای قرار میگیرد: در افراد مبتلا به مرض قند که تمایل به خوردن مربا یا شربت شیرین دارند میتوان از سوریبتول استفاده کرد. زیرا به علت جذب کند سوریبتول مقداری از این مواد وارد روده شده و توسط فلور روده تخمیر میشود و گاز ایجاد میکند.بنابراین فرد مبتلا به مرض قند میتواند دو قاشق مرباخوری سوربیتول بخورد و اگر مقدار زیادتری استفاده کند دچار نفخ میشود و اگر مقدار بیشتری استفاده کند دچار اسهال میشود. یکی از مشکلات افرادی که رژیم لاغری میگیرند، پائین آمدن قند خون و احساس گرسنگی است. بنابراین سوریبتول درست است که کربوهیدرات است اما به دلیل جذب کُند، مصرف مقدار کمی از آن میتواند قند خون را در حد طبیعی نگه دارد و یا در افرادی که در ذخیره سازی گلیکوژن کبدی مشکل دارند، میتوان از این ویژگی بهره جست. مشتقات تک قندی به نام اینوزیتول، که یک هکزوز حلقوی است، معمولاً در سبوس غلات مثل نان به صورت ترکیب با شش مولکول اسید فسفوریک است که اصطلاحاً به آن اسید فیتیک میگویند. وقتی اسید فیتیک بدین صورت است، ارزش تغذیهای ندارد زیرا قند و فسفر آن قابل استفاده نیست و در ضمن مانع جذب کلسیم و آهن غذا نیز میشود، اما اگر نانی مثل نان سنگک را تخمیر کنیم به وسیله خمیر ترش اسید فیتیک تجزیه میشود، قند و فسفر آن قابل استفاده میگردد و مانع از جذب کلسیم و فسفر هم نمیشود.
تست مولیش :
Shows positive test for:
All carbohydrates. Monosaccharides give a rapid positive test. Disaccharides and polysaccharides react slower.
Reactions:
The test reagent dehydrates pentoses to form furfural (top reaction) and dehydrates hexoses to form 5-hydroxymethyl furfural (bottom reaction). The furfurals further react with  -naphthol present in the test reagent to produce a purple product (reaction not shown).
-naphthol present in the test reagent to produce a purple product (reaction not shown).


How to perform the test:
Two ml of a sample solution is placed in a test tube. Two drops of the Molisch reagent (a solution of  -napthol in 95% ethanol) is added. The solution is then poured slowly into a tube containing two ml of concentrated sulfuric acid so that two layers form.
-napthol in 95% ethanol) is added. The solution is then poured slowly into a tube containing two ml of concentrated sulfuric acid so that two layers form.
A positive test is indicated by:
The formation of a purple product at the interface of the two layers.

تست بارفورد :
Shows positive test for:
Reducing monosaccharides
Reactions:
Reducing monosaccharides are oxidized by the copper ion in solution to form a carboxylic acid and a reddish precipitate of copper (I) oxide within three minutes. Reducing disaccharides undergo the same reaction, but do so at a slower rate.

How to perform the test:
One ml of a sample solution is placed in a test tube. Three ml of Barfoed's reagent (a solution of cupric acetate and acetic acid) is added. The solution is then heated in a boiling water bath for three minutes.
A positive test is indicated by:
The formation of a reddish precipitate within three minutes.

تست بندیکت :
Carbohydrate

Procedure
To a solution or suspension of 0.2 g of unknown in 5 mL of water, add 5 mL of Benedict's solution. If no precipitate is formed, heat the mixture to boiling and cool.
Benedict's solution: A solution of 17.3 g of sodium citrate and 10.0 g of anhydrous sodium carbonate in 80.0 mL of water is heated until the salts are dissolved. Additional water is added to bring the volume up to 85.0 mL. A solution of 1.73 g of hydrated copper sulfate in 10.0 mL of water is poured slowly with stirring into the solution of the citrate and the carbonate. Add water to make a final volume of 100 mL.
Positive Test
Precipitation of copper(I) oxide as a red, yellow, or yellowish-green solid is a positive test.
Complications
Not general for simple aldehydes and ketones.
Hydrazine derivatives give a positive test.
تست باروکس :

Procedure
In a test tube, a few drops of phenolphthalein are added to 0.5 mL of a 1% solution of borax. A pink solution is formed. A couple of drops or a few crystals of the unknown are added. If the pink color begins to fade after the unknown and the reagent have been mixed together, then continue to add small amounts of the unknown until the pink color fades completely. Place the test tube in a hot water bath. If the pink color reappears on warming, and dissipates again on cooling, then the unknown is a polyhydric alcohol.
Positive Test
Carbohydrates and 1,2-diols give a positive test.
Complications
None.
تست اوسازون :

Procedure
Place 0.2 g of the unknown sample in a test tube and add 0.4 g of phenylhydrazine hydrochloride, 0.6 g of crystallized sodium acetate, and 4 mL of distilled water. Place the test tube in a beaker of boiling water. Note the time that the test tube was immersed and the time of the precipitation. After 20 min, remove the test tube from the hot water bath and set it aside to cool. A small amount of the liquid and solid is poured on a watch glass. Tip the watch glass from side to side to spread out the crystals, and absorb some of the mother liquid with a piece of filter paper, taking care not to crush or break up the clumps of crystals. Examine the crystals under a low-power microscope (about 80-100×), and compare with photomicrographs. The formation of tarry products due to oxidation of the phenylhydrazine may be prevented by the addition of 0.5 mL of saturated sodium bisulfite solution. This should be done before heating if it is desired to isolate the osazone and determine its melting point.
Positive Test
Carbohydrates and 1,2-diols give a positive test.
Complications
The times required for the formation of the osazones can be a valuable aid in distinguishing among various sugars. The following figures are the times required for the osazone to precipitate from the hot solution: fructose, 2 min; glucose, 4-5 min; xylose, 7 min; arabinose, 10 min; galactose, 15-19 min; raffinose, 60 min; lactose, osazone soluble in hot water; maltose, osazone soluble in hot water; mannose, 0.5 min (hydrazone); sucrose, 30 min (owing to hydrolysis and formation of glucosazone).
Osazone formation involves hydrazone formation at C-1 of an aldose (or C-2 of a ketose) and oxidation of C-2 (or C-1) of an alcohol group to a ketone (or an aldehyde). The new carbonyl group is also converted to a hydrazone. It has been suggested that the reaction stops here (rather than further oxidation at C-3, etc.) because of hydrogen-bonding stabilization of the osazone.
نقطه ذوب دمایی است که جامد به مایع تبدیل و یا دمایی که در ان فشار بخار مایع و جامد برابرند .زمانیکه یک جامد در اثر حرارت ذوب میگردد با پدیدارشدن مایع بین مایع و جامد تعادل برقرار می گردد و ادامه گرما باعث تبدیل جامد به مایع می گردد. معمولا ماده الی خالص دارای نقطه ذوب معین و بسیار سریع می باشد.
وجود مقدار کم ناخالصی نقطه ذوب را تغییر می دهد لذا داشتن نقطه ذوب جسم خالص ونتیجه حاصله از یک ازمایش خلوص جسم را تعیین می کند .( در این مورد استسنائاتی هم وجود دارد )
روش میکرو
یک لوله موئین به طول 7 – 5 سانتی متر برداشته یک دهانه ان را با استفاده از شعله مسدود کنید.
نمونه جامد مورد نظر را کاملا پودر کرده و وارد لوله موئین کنید ( لوله موئین 5 – 7 سانتی متر پر شود )
لوله موئین را طوری به ترمومتر متصل نمایید که انتهای لوله و ترمومتر هم سطح باشند ( این کار را به کمک سیم یا حلقه نازک و کوچک لاستیکی انجام دهید ولی نباید در حمام قرار گیرد )
ترمومتر اماده شده را به کمک گیره و پایه طوری به حالت اویزان درون حمام قرار دهید که مخزن ترمومتر و ماده جامد درون مایع قرار گیرند .( مایع حمام معمولا از پارافین – گلی کول – گلیسیرین – اسید سولفوریک غلیظ که نقطه جوش بالایی دارند استفاده میشود)
سپس حمام را به ارامی حرارت دهید به طوری که ماکزیمم هر یک دقیقه دو درجه سانتیگراد بالا رود. دمای شروع نقطه ذوب و دمایی که در ان اخرین قسمت جامد دوب میگردد را یاداشت کنید. تفاضل این دو عدد را در اصطلاح دامنه ذوب می گویند .
دامنه ذوب ترکیبات خالص معمولا 2 – 0.5 درجه سانتیگراد است.

روش ماکرو
دمای ذوب را می توان به روش ماکرو بدست اورد و ملاحظه نمود که در طول ذوب دما ثابت است .انواع دستگاههای ساده الکتریکی برای تعیین نقطه ذوب ترکیبات الی به روش ماکرو وجود دارد .
نقطه جوش دمائی است که در ان فشار بخار مایع برابر فشار بخار جو می گردد لذا برای ثبت نقاط جوش ذکر فشار خارجی را می طلبد و زمانیکه فشار ذکر نشود منظور نقطه جوش در فشار یک اتمسفر کامل می باشد که نقطه جوش نرمال نامیده میشود .
بعضی از مایعات قبل از رسیدن به نقطه جوش تجزیه می شوند .
روش اندازگیری نقطه جوش به مقدار مایعی که در اختیار داریم بستگی دارد اگر مقدار زیاد باشد از روش تقطیر و اگر کم باشد از روش میکرو استفاده میشود .
روش میکرو
انتهای لوله موئین را به کمک شعله مسدود کنید و به طول یک سانتیمتر بشکنید و از طرف دهانه باز ان را دریک لوله ازمایش خشک و تمیز از جنس شیشه نازک به قطر 7 – 5 میلی متر وارد کنید.
داخل لوله ازمایش مایعی را که میخواهید نقطه جوش بگیرید انقدر بریزید که لوله موئین را بپوشاند .
لوله ازمایش را با کمک سیم یا لاستیک به ترمومتر متصل کنید به طوری که مخزن ترمومتر در کنار مایع داخل لوله ازمایش باشد.
ترمومتر را به کمک گیره و پایه طوری متصل نمایید که مخزن ترمومتر و مایع داخل لوله ازمایش داخل حمام قرار گیرد.
سپس حمام را به ارامی و با شعله متوسط گرم نمایید تا حباب های پیوسته از لوله موئین خارج شود در این هنگام حرارت را قطع نمایید تا حمام سرد شود .
خروج حباب از لوله موئین به تدریج کم خواهد شد تا زمانی که دیگر حبابی خارج نمی شود و مایع وارد لوله موئین میشود و داخل لوله موئین بالا میرود .
زمانی که حباب ها قطع میشود فورا دمای ترمومتر را خوانده که دمای جوش مایع می باشد .
برای کاهش خطا در ازمایش فوق میتوان پس از خواندن دمای جوش مایع حمام را مجددا گرم نمود تا حباب های پیوسته از لوله موئین خارج شود و سپس حرارت را قطع کرده و هنگامی که خروج حباب ها پایان یافت دمای جوش را مجدد خواند.