 |
|
|
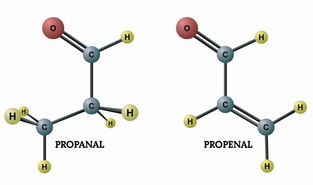
کلمه آلدئید (Aldehyde) از دو واژه الکل (Alcohal) و هیدروژنگیری (dehydrogenation) گرفته شده است. هرگاه از الکل نوع اول هیدروژنگیری شود، در آن صورت ، ماده ای تولید میگردد که آلدئید نامیده میشود.
نامگذاری آلدئیدها
در نامگذاری قدیمی ، نام آلدئید از نام اسید آلی مربوطه آن گرفته میشد. مثلا آلدئید فرمیک از اسید فرمیک ، آلدئید استیک را از اسید استیک و آلدئید پروپیونیک از اسید پروپیونیک بوجود آمده است. در نامگذاری جدیدی برای نامگذاری آلدئیدها ، ابتدا طولانیترین زنجیر حاوی عامل آلدئیدی را انتخاب میشود و سپس شماره گذاری اتمهای کربن از جهتی که گروه آلدئیدی قرار گرفته است، انجام میگیرد. برای نامگذاری ، ابتدا شماره و نام شاخههای فرعی را نوشته ، در پایان ، اسم هیدروکربن را بطور کامل ذکر و پسوند آل (al) بر آخر آن افزوده میشود.
تهیه آلدئیدها از اکسید گردن الکلهای نوع اول
با استفاده از برخی اکسید کنندههای ملایم مثل دیاکسیدمنگنز ، واکنشگر CrO3/H+/CH3COCH3) Jones) یا واکنشگر CrO3/HCl/Pyridine) Sarett) یا واکنشگر (CrO3/2pyridine/CH2Cl2) و کرومیل کلرید Cr2Cl2 ، الکل های نوع اول و دوم بصورت محدود اکسید میشوند.
الکل های نوع اول به آلدئید و نوع دوم به کتون هم کربن خود تبدیل میگردند.
تهیه آلدئیدها و کتونها با استفاده از ترکیبات آلی فلزی
گاهی اوقات از ترکیبات آلی فلزی برای سنتز آلدئیدها و کتونها استفاده میشود. در سالهای اخیر ، برای سنتز ترکیبات کربونیلدار از R2Cd یا RZnX یا R2Zn استفاده زیاد شده است. قدرت هسته خواهی ملایم و محدود این واکنشگرها این امکان را فراهم میکند که از کلرواسیدها ، کتونهای مربوطه سنتز شود.
تهیه آلدئیدها از اورگانومنیزینها
از فعل و انفعال اورگانومنیزینها با نیتریلها و آمیدها نیز میتوان آلدئید و کتون تهیه نمود. البته برای تهیه آلدئید باید آمید به شکل فرم آمید باشد.
سنتز آلدئیدها از واکنش آلکوکسی هیدریدلیتیم آلومینیوم با آمیدها و کلرواسیدها
احیای کلرواسیدها و آمیدها به کمک هیدریدیهای مناسب از قبیل تریآلکوکسی هیدرید لیتیم آلومینیوم به تشکیل آلدئید مربوطه منجر میگردد. توجه به این نکته ضرورت دارد که احیای کلرواسیدها بوسیله تریترسیو بوتوکسی لیتیم آلومینیوم در دمای پایین در حدود 78- درجه سانتیگراد و در حلالهای مناسب مانند دیگلایم MeO-CH2-CH2-O-CH2-CH2-OMe انجام میشود.
برای تبدیل آمیدها به آلدئیدهای مربوط ، از دیآلکوکسی هیدرید لیتیم آلومینیوم نیز میتوان استفاده کرد.
تهیه آلدئیدها از طریق هیدروفرمیه کردن آلکنها
آلکنها در حضور کاتالیزور تریستری فنیل فسفین رودیم کلراید با هیدروژن و منوکسید کربن ترکیب و به تشکیل آلدئید منجر میشود. با توجه به اینکه در این واکنش به یکی از کربنهای پیوند دوگانه ، هیدروژن و به کربن دیگر ، عامل آلدئیدی (-CHO) متصل میشود، لذا این واکنش را هیدروفرمیله شدن میگویند. در حضور کاتالیزور ذکر شده فقط یک نوع آلدئید تولید میشود. هر گاه از اکتا کربونیل دیکبالت به عنوان کاتالیزور استفاده شود، دو نوع ایزومر تولید میشود.
تهیه آلدئیدها از نیتریلها
در دمای پایین ، نیتریلها با هیدریدلیتیم آلومینیوم ترکیب میشوند و کمپلکس حد واسط را تشکیل میدهند. این کمپلکس در حضور محلول اسید هیدرولیز میشود و آلدئید مربوطه را تولید میکند.
سنتز آلدئیدهای آروماتیک با استفاده از واکنش کاترمن
یکی از روشهای تهیه آلدئیدهای آروماتیک این است که در حضور یک اسید لوئیس مناسب مثل کلروآلومینیوم یا کلرید روی ، سیانید هیدروژن و کلرید هیدروژن با ترکیبات آروماتیک واکنش داده شوند.
سنتز آلدئیدهای آروماتیک با استفاده از دیمتیل فرمآمید فسفریل کلراید
از اختلاط اکسی تریکلرو فسفر با فرمآمید ، کمپلکس تشکیل میشود که به دیمتیل فرمآمید فسفریل کلراید موسوم است و میتواند در واکنشهای جانشینی الکترونخواهی آروماتیک شرکت نماید. با این روش حتما آلدئیدهای هتروسیکلهایی مانند تیوفن و فوران نیز سنتز شدهاند.
سنتز آلدئیدهای آروماتیک از فنل ها و کلروفرم در حضور هیدروکسید سدیم
با استفاده از واکنش کلروفرم قلیایی شده با فنلها و از طریق جانشینی الکترونخواهی دیکلرو کاربن روی حلقه آروماتیک میتوان آلدئید سنتز نمود.
 |
|
|
خواص شیمیایی آلدئیدها و کتون ها
آلدئیدها و کتونها در چند نوع فعل و انفعال شرکت میکنند که اهم آنها به قرار زیر است:
-
حمله الکترونخواهی اسیدهای لوئیس روی اکسیژن گروه کربونیل ، موجب افزایش دانسیته بار مثبت کربن گروه کربونیل میشود که در نهایت ، موجب افزایش خصلت اسیدی پروتونهای کربنهای آلفای کربونیل میگردد. صحت این نکته بوسیله روشهای افزاری تایید شده است. به عنوان مثال ، محلولی از استن و سوپراسید (SbCl5 , FSO3H ) در دیاکسید سولفور مایع و در60- درجه سانتیگراد بوسیله n.m.r مطالعه و مشاهده شده است که جذب پروتونهای استن در میدانهای ضعیفتری صورت میگیرد.
-
حمله هستهخواهی بر کربن گروه کربونیل ، دومین دسته وسیع از واکنشهای آلدئیدها و کتونها را تشکیل میدهد. به عنوان مثال ، از افزایش آب بر آلدئیدها و کتونها ، دیول دو قلو (gemdiol) ایجاد میشود و درصد تشکیل آن به ساختمان ماده و به پایداری محصول حاصل بستگی دارد. به عنوان مثال ، مقدار دیول دو قلوی حاصل از استون در دمای 20 درجه سانتیگراد خیلی کم و قابل اغماض میباشد، درصورتی که آلدئید فرمیک و تریکلرو استالدئید بخوبی و بطور کامل به دیول دوقلو مربوط به تبدیل میشوند.
۱- (2 و 4- دي نيتروفنيل هيدرازين) 

غالب آلدهيدها و کتونها در واکنش با 2 و 4- دي نيتروفنيل هيدرازين رسوب نارنجي مايل به قرمز تشکيل مي دهند، اما فقط آلدهيدها مي توانند کرومIV و نقره (I) را کاهش دهند. اين تفاوت واکنش پذيري به عنوان وجه تمايز بين آلدهيدها و کتونها است.
يک قطره از مايع مجهول را در يک لوله آزمايش کوچک بريزيد و يک ميلي ليتر واکنشگر 2 و 4- دي نيتروفنيل هيدرازين به آن اضافه کنيد. چنانچه مجهول جامد است حدود 10 ميلي گرم از آنرا در حداقل مقدار اتانول (95 %) يا دي اکسان حل کنيد سپس واکنشگر را به آن بيافزاييد، لوله آزمايش محتوي مخلوط را به شدت تکان دهيد. غالب آلدهيدها و کتونها فوراً رسوبي به رنگ زرد تا قرمز توليد مي کنند. اما براي بعضي ترکيبات براي تشکيل رسوب بايد 15 دقيقه صبر کرد و يا به آرامي آنرا حرارت داد. تشکيل رسوب به منزله مثبت بودن اين آزمايش است.
تهيه واکنشگر
3 گرم (2 و 4- دي نيتروفنيل هيدرازين) در 15 ميلي ليتر سولفوريک اسيد غليظ بريزيد. در يک بشر 20 ميلي ليتر آب و 70 ميلي ليتر اتانول 95 % ريخته در حاليکه آنرا به شدت بهم زنيد آهسته محلول 2 و 4-دي نيتروفنيل هيدرازين را به مخلوط آبي اتانول اضافه نماييد. بعد از مخلوط کردن محلول را روي کاغذ صافي چين دار صاف کنيد. محلول صاف شده، معرف آماده براي واکنش است.
2- کروميک اسيد
يک قطره يا حدود 10 ميلي گرم (اگر مجهول جامد است) از نمونه را در يک ميلي ليتر استون (خالص براي واکنش) حل نماييد. چند قطره از واکنشگر کروميک اسيد اضافه کنيد، بدين ترتيب که يک قطره اضافه کنيد و بهم بزنيد سپس قطره بعدي را اضافه کنيد. چنانچه رسوب سبز رنگ تشکيل شود و رنگ نارنجي معرف از بين برود دليل بر مثبت بودن نتيجه آزمايش است. براي آلدهيدهاي آليفاتيک (RCHO) محلول براي 5 ثانيه کدر مي شود و پس از 30 ثانيه رسوب ظاهر مي شود.آلدهيدهاي آروماتيک (ArCHO) پس از (120 – 30) ثانيه رسوب مي دهند. اما بعضي موارد تشکيل رسوب پس از زمان بيشتري رؤيت مي شود. وقتي نتيجه آزمايش منفي است رسوب تشکيل نمي شود. اما، در بعضي موارد، رسوبي ديده مي شود اما رنگ نارنجي معرف باقي مي ماند.
در هنگام انجام اين آزمايش، بايد از خلوص استون اطمينان حاصل نماييد در غير اينصورت با واکنشگر واکنش مي دهد و نتيجه مثبت براي آن حاصل مي شود. لذا قبل از انجام آزمايش به لوله آزمايش کوچکي که محتوي استون است چند قطره کروميک اسيد اضافه کنيد و پس از مخلوط کردن 5-3 دقيقه صبر کنيد. اگر بعد از اين مدت واکنشي انجام نشده بود در اينصورت استون از خلوص کامل برخوردار است. چنانچه نتيجه آزمايش مثبت بود، از بطري استون ديگر استفاده کنيد و يا در استون مقداري پتاسيم پرمنگنات بريزيد و سپس تقطير کنيد و استون تقطير شده را که خالص است براي آزمايش بکار ببريد.
تهيه واکنشگر
يک گرم کروميک اسيد (CrO3) را در يک ميلي ليتر سولفوريک اسيد غليظ حل کنيد. سپس مخلوط را با دقت با 3 ميلي ليتر آب رقيق نماييد.
اين آزمايش در صورتي براي شناسايي آلدهيد سودمند است که شناسايي گروه کربونيل آن به وسيله واکنشگر 2 و 4- دي نيترو فنيل هيدرازين تأييد شده باشد. الکلها به اين واکنشگر پاسخ مثبت نمي دهند. اما به معرف کروميک اسيد جواب، مثبت مي دهند.
3- آزمايش تالنز
غالب آلدهيدها با محلول 
 نقره نيترات آمونياکي واکنش مي دهند و نقره رسوب مي کند (آئينه نقره يي). کتونهاي معمولي به اين واکنشگر جواب نمي دهند. واکنشگر بايد بلافاصله قبل از مصرف تهيه شود. براي تهيه واکنشگر، يک ميلي ليتر از محلول تولنس (A) را با يک ميلي ليتر محلول تولنس (B) مخلوط مي کنيم. رسوب نقره اکسيد تشکيل مي شود و سپس قطره قطره محلول آمونياک را به مخلوط اضافه کنيد تا رسوب اکسيد نقره حل شود. اکنون واکنشگر براي انجام آزمايش را آماده است.
نقره نيترات آمونياکي واکنش مي دهند و نقره رسوب مي کند (آئينه نقره يي). کتونهاي معمولي به اين واکنشگر جواب نمي دهند. واکنشگر بايد بلافاصله قبل از مصرف تهيه شود. براي تهيه واکنشگر، يک ميلي ليتر از محلول تولنس (A) را با يک ميلي ليتر محلول تولنس (B) مخلوط مي کنيم. رسوب نقره اکسيد تشکيل مي شود و سپس قطره قطره محلول آمونياک را به مخلوط اضافه کنيد تا رسوب اکسيد نقره حل شود. اکنون واکنشگر براي انجام آزمايش را آماده است.
يک قطره از آلدهيد مايع يا 10 ميلي گرم اگر آلدهيد جامد است. در حداقل مقدار دي اکسان حل نمايند. اين محلول را به 2 يا 3 ميلي ليتر از واکنشگر که در لوله آزمايش کوچکي قرار دارد اضافه کنيد. محلول را خوب مخلوط کنيد. اگر رسوب نقره روي ديواره لوله تشکيل شد جواب آزمايش مثبت است. در بعضي موارد براي تشکيل رسوب نقره (آئينه نقره يي) لازم است لوله آزمايش را در حمام آب گرم قرار داد.
توجه : واکنشگر تولنس بايد در هنگام مصرف تهيه شود و هر چه باقي مي ماند بايد بلافاصله همراه با آب زياد و در ظرفشويي بريزيد. چنانچه محلول نگهداري شود امکان تشکيل نقره فولمينات (Ag2C2N2O2) که ماده بسيار انفجار پذيري است، وجود دارد. بنابراين واکنشگر تولنس را هرگز نبايد از قبل تهيه و نگهداري کرد.
تهيه واکنشگر
محلول A از حل کردن 3 گرم نقره نيترات در 30 ميلي ليتر آب قابل تهيه است. محلول B، محلول سديم هيدروکسيد 10 % است.
4- آزمايش يدوفرم
اين آزمايش براي شناسايي متيل کتونها و ترکيباتيکه در اثر شرايط واکنش اکسيد شوند و به – Co – CH3 تبديل شوند، انجام پذير است، گروههاي ,-CH3CO CHI2CO- ,CH2ICOبه آزمايش يدوفرم پاسخ مثبت مي دهند. براي واکنش وجود يک هيدروژن فعال در اتصال به کربني که فاقد ممانعت فضايي باشد لازم است. ترکيبات CH3CO - COCH3 , RCO - CH2 - CO - R , CH3CHOHR , CH3COR , CH3CH2OH CH3CHO نسبت به واکنش يدوفرم واکنش پذيري دارند و رسوب زرد يدوفرم تشکيل مي دهند.
4 قطره از مجهول مايع يا 1/0 گرم از مجهول جامد با 3 ميلي ليتر آب را در يک لوله آزمايش بزرگ (mm15*8/1) حل نماييد. چنانچه مجهول در آب حل نمي شود براي انحلال مجهول از 3 ميلي ليتر دي اکسان به جاي آب استفاده نماييد. و يک ميلي ليتر محلول سديم هيدروکسيد 10 % به آن مخلوط اضافه کنيد. سپس قطره قطره محلول يد – پتاسيم يديد در حاليکه بهم مي زنيد به مخلوط اضافه نماييد و بهم بزنيد افزايش يد را تا وقتي که رنگ قهوه يي محلول باقي بماند ادامه دهيد. رنگ يد اضافي را با اضافه کردن سود بصورت قطره قطره به همراه تکان دادن از بين ببريد. لوله را از آب پر کنيد و بگذاريد 15 دقيقه بماند. اگر ترکيب متيل کتون باشد يا در اثر شرايط اکسيد کنندگي، ملکول به متيل کتون تبديل شده باشد، رسوب زرد يدوفرم تشکيل مي شود. براي تأييد تشکيل رسوب يدوفرم، رسوب را صاف کنيد و پس از خشک کردن نقطه ذوب آنرا تعيين نماييد (نقطه ذوب يدوفرم ˚121-119 است) در صورت مصرف بيش از اندازه دي اکسان، يدوفرم را حل مي نمايد، افزايش آب به همين دليل است.
تهيه واکنشگر
20 گرم پتاسيم يديد و 10 گرم يد را در 100 ميلي ليتر آب حل نماييد.
۵-تست فوشین
این تست به الدهیدها و کتونهای سبک جواب مثبت داده و ارغوانی رنگ میشود
Protein Carbonyl Determination Using Biotin Hydrazide
Tollens Reaction - Silver Mirror Test
Fuchsin-Aldehyde Reagent (Schiff's Reagent)
2,4-Dinitrophenylhydrazine Test for Carbonyl Compounds
Addition of Bisulfite to Cyclohexanone
Iodoform Test for Methyl Ketones
كتون:(ketone)
یک کتون یک گروه عاملی است که با یک گروه کربونیل که با دو اتم کربن دیگر پیوند دارد ؛ شناخته میشود. یک کتون را میتوان با فرمول R۱(CO)R۲ بیان کرد. اتم کربن که با دو اتم کربن پیوند دارد آن را از گروههای عاملی کربوکسیلیک اسیدها ، آلدهیدها، استرها، آمیدها و دیگر ترکیبهای اکسیژندار جدا میکند. پیوند دوگانهٔ گروه کربونیل نیز کتونها را از الکل ها و اترها باز میشناساند.
به کربنی که به کربن گروه کربونیل چسبیده کربن آلفا و به هیدروژنی که به این کربن چسبیده هیدروژن آلفا گویند. در حضور یک کاتالیزور اسیدی کتون به keto-enol tautomerism مربوط میشود. واکنش با یک پایه قوی انول متناظر را نتیجه میدهد.
خواص شیمیایی آلدهید ها و كتون ها:
آلدهید ها وكتون ها در چند نوع فعل و انفعال شركت می كنند كه اهم آن به قرار زیر است:
1)حمله الكترونخواهی اسیدهای لوئیس روی اكسیژن گروه كربونیل موجب افزایش دانسیته بار مثبت كربن گروه كربونیل می شود كه در نهایت موجب افزایش خصلت اسیدی پروتون ههای كربن های آلفای كربونیل می گردد.صحت این نكته به وسیله روش های افزاری تائید شده است.
2)حمله هسته خواهی بركربن گروه كربونیل دومین دسته وسیع از واكنشهای آلدهید ها وكتون ها را تشكیل می دهد.به عنوان مثال از افزایش آب بر آلدهید ها وكتون ها دیول دوقلو(gemdiol)ایجاد می شود و درصد تشكیل آن به ساختمان ماده و به پایداری محصول حاصل بستگی دارد.به عنوان مثال مقدار دیول دوقلوی حاصل از استون در دمای 20درجه سانتی گراد خیلی كم و قابل اغماض است در صورتیكه آلدهید فرمیك و تری كلرو استالدهید به خوبی و به طور كامل به دیول دو قلو تبدیل می شوند.
تهیه آلدهید ها و كتون ها از راه اكسایش الكل ها:
مصرف زیاد آلدهید و كتون در سنتزهای آلی باعث می شود كه نحوه تهیه آنها اهمیت بسیاری داشته باشد.این اجسام را می توان از آلكین ها –كربوكسیلیك اسیدها و مشتق كربوكسیلیك اسیدها سنتز كرد.آلكینها دراثرآبداركردن باكاتالیزور اسید به وسیله هیدروبورداركردن-اكسایش به آلدهید یا كتون تبدیل می شوند.
كربوكسیلیك اسیدها یا مشتقات آنها با تركیبات آلی فلزدار یا معرف های كاهند دیگر تركیب می شوند و آلدهید یا كتون می دهند.با وجود این یكی از معمولترین روش های سنتزی اكسایش الكل های نوع اول و دوم با كرومیك اسید H2CrO4 یا پتاسیم پرمنگنات است.
در این گزارش كار نحوه مصرف كرومیك اسید در تبدیل الكلها به آلدهید ها و كتون ها مورد بحث قرار می گیرد.
كرومیك اسید برای مدت طولانی پایدار نیست و بنابراین آن را در هنگام لزوم از تركیب سدیم یا پتاسیم دی كرومات با اسید اضافی مانند سولفوریك یا اسد استیك یا با انحلال كرومیك انیدرید در آب تهیه می كنند.
در روش اخیر سولفوریك اسید یا استیك اسید نیز اضافه می شود زیرا كه سرعت اكسایش الكل ها با كرومیك اسید در محلول اسیدی بسیار زیادتر است.در تهیه یا اكسایش اجسامی كه در محیط اسیدی قوی تجزیه می شوند كرومیك انیدریدرا در پیریدین حل می كنند یا پتاسیم پرمنگنات بازی را به عنوان معرف اكسید كننده به كار می برند.
الكلها در مجاورت كرومیك اسید به استر تبدیل می شوند.این عمل كاملا به واكنش الكل ها وكربوكسیلیك اسیدها شباهت دارد.
وجود چند واكنش جانبی مهم اكسایش الكل نوع اول به آلدهید را پیچیده می كند.
به احتمال زیاد مهمترین واكنش جانبی اكسایش سریع آلدهید با كرومیك اسید و تبدیل آن به كربوكسیلیك اسید است.برای تقلیل این اكسایش اضافی نامطلوب كرومیك اسید را به الكل نوع اول اضافه می كنند تا عامل اكسنده اضافی در مخلوط واكنش موجود نباشد وهم چنین آلدهیدرا در هنگام تشكیل از مخلوط واكنش تقطیر می كنند.بنابراین چنان چه در اكسایش با كرو میك اسید لازم باشد كه آلدهید با بازده زیادی تهیه می شودباید آلدهید موردنظر خیلی فرارباشد یعنی در كمتر از حدود 150بجوشد.
كتون ها در محیط اسیدی ملایم در برابر این اكسنده بسیار پایدارتر از آلدهیدها هستند از این رو در تبدیل الكل های نوع دوم به كتون ها میزان واكنش های جانبی كه در اكسایش الكل های نوع اول گفته شد چندان قابل ملاحظه نیستند.ولی در شرایط بازی یا اسیدی قوی كتون هایی كه به فرم انولی در می آیند اكسید می شوند و به دو قسمت كربونیل دار تجزیه می شوند.برای مثال می توان سیكلو هگزانول را با كرومیك اسید اكسیدكرد وبازده زیادی از سیكلوهگزانون به دست آورد ولی این جسم در اثر تركیب با پتاسیم پرمنگنات در محیط بازی ضعیف به آدیپیك اسید تبدیل می شود.بدون شك در این واكنش ابتدا كتون به یون انولات تبدیل می شود تبدیل می شودو بعداین یون با پرمنگنات اكسید می شود.
سیكلوهگزانون یك كتون متقارن است و فقط یك یون انولات می دهد.چنان چه كتون متقارن نباشد دو یون انولات متفاوت تولی می شود وهر یك از آنها با پرمنگنات به محصول جداگانه ای اكسید می شود.در اكسایش كتون های نامتقارن مخلوط پیچیده ای از چند محصول تشكیل می شود وچنین مشكلی مصرف سنتزی این واكنش ها را كم می كند.
روشهای تهیه آلدهید و کتون:

واکنش آلدئیدها و کتون





مثالهایی از واکنش آلدهید و کتون ها:

